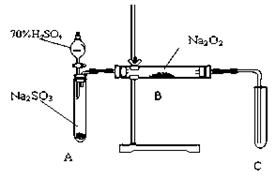
(15分)化学兴趣小组同学运用类比学习的思想,探究过氧化钠与二氧化硫的反应。小组同学改进了下图所示的装置进行实验制取SO2的反应。充分反应,B中固体由淡黄色变为白色(Na2O2完全反应),将带火星的木条插入试管C中,木条复燃。试回答下列问题:
(3)  请你完成装置改进的措施和理由:
请你完成装置改进的措施和理由:
 ①措施:在A、B之间加一个干燥管,
①措施:在A、B之间加一个干燥管, 作用_______________________________________。
作用_______________________________________。
 ②措施:为确保C中的实验现象发生,在B、C之间加一个装有_________________的洗气瓶,
②措施:为确保C中的实验现象发生,在B、C之间加一个装有_________________的洗气瓶, 作用_______________________。
作用_______________________。
(2)某同学推断该白色固体为Na2SO3,则其化学反应方程式是____________________________。
(3)任何的推论都要经过检验,请完成对白色固体成分的探究:
限选实验仪器与试剂:烧杯、试管、药匙、滴管、酒精灯、带单孔胶塞的导管、棉花、试管夹;3 mol·L-1HCl、6 mol·L-1HNO3、NaOH稀溶液、蒸馏水、1 mol·L-1 BaCl2溶液、澄清石灰水、品红溶液。
① 提出合理假设:
假设1:白色固体为Na2SO3; 假设2: ;
假设3:白色固体为Na2SO3与Na2SO4的混合物。
② 设计实验方案证明以上三种假设,并按下表格式写出实验操作步骤、预期现象与结论。
| 实验操作 | 预期现象与结论 |
| 步骤1:取少量白色固体于试管,加入 ,塞上单孔胶塞,将生成的气体通入 。 | 若 ,说明白色固体含有Na2SO3,则 成立,若无该现象, 则 成立。 |
| 步骤2:在步骤1反应后的溶液加入 。 | 若 ,则说明白色固体含Na2SO4。 结合步骤1的结论,则 成立,若无该现象,则 则 成立。 |
(1) ①产生的二氧化硫没有干燥,水蒸气会与Na2O2反应;
②NaOH溶液 除去SO2气体,防止污染空气
(2) 2Na2O2+2SO2=2Na2SO3+O2(2分)
(3)①提出合理假设
假设3:白色固体为Na2SO4
②
| 实验操作 | 预期现象与结论 |
| 步骤1:取少量白色固体于试管,加入过量3 mol·L-1的稀盐酸,塞上单孔胶塞,将生成的气体通入品红溶液。 | 若有能使品红溶液褪色的无色气体生成,说明白色固体含有Na2SO3。则假设1或3成立,若无该现象,则假设2成立。 |
| 步骤2:在步骤1反应后的溶液加入1 mol·L-1 BaCl2溶液。 | 若有白色沉淀生成,则说明白色固体含Na2SO4。结合步骤1的结论,则假设3成立,若无该现象,则假设1成立。 |
题目分析:(1)2Na2O2+2H2O=4NaOH+O2↑二氧化硫是有毒气体,实验中要除去以防污染空气。(2)由CO2与Na2O2的反应,生成了Na2SO3和O2,化学方程式为2Na2O2+2SO2═2Na2SO3+O2。(3)要证明白色固体中含有Na2SO3只需检验出含有SO32-就可以了,取少量白色固体,加入稀硫酸或稀盐酸,产生能使品红溶液褪色的气体,则证明生成的白色固体中含有Na2SO3。2O2性质,物质的检验
点评:本题为研究性试题,以探究过氧化钠与二氧化硫的反应为依托,考查知识的迁移能力、设计和评价实验方案的能力
