| 完形填空。 | ||||
| Hello, I am Tom. I am a middle school student. It's nice to meet you here. First, let me tell you something 1 my family. There are five people in my 2 . They are my mother, my father, my sister, my brother and me. My father is a policeman. My mother is 3 English teacher. My sister is eighteen and my brother is sixteen. I'm fourteen. We all go to the same school. We all enjoy 4 football games. My 5 is at West Street. There is a big tree and some small trees around my house. The big 6 is a pear tree and the small ones are apple trees, but there 7 any pears or apples 8 them now. 9 a photo of my house. In the photo, you can see two cats in my house. They are both black and white. We 10 them very much. | ||||
|
1-5: BDCCC 6-10: BDBDC

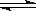 FeO(s)+CO(g)的平衡常数为K1。
FeO(s)+CO(g)的平衡常数为K1。