某化学兴趣小组为探究SO2的性质,查阅相关资料知:实验室制取SO2气体的反应原理为Na2SO3 + H2SO4  Na2SO4 + SO2↑+ H2O,据此设计如下图所示装置进行相关实验。
Na2SO4 + SO2↑+ H2O,据此设计如下图所示装置进行相关实验。
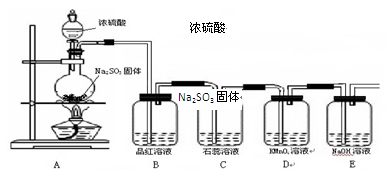
|
(1)盛装浓硫酸的仪器的名称是 。
(2)按上图连接好装置再 (填操作名称),然后加入试剂并加热。
(3)实验过程中, 装置B、C中可观察到的实验现象分别是 、 。
(4)D中可观察到的现象是_______________,说明SO2具有 性。
(5)装置E的作用是 。
(1)分液漏斗 (2 分) (2)检查装置的气密性。(2 分)
(3)品红溶液褪色(1分) 石蕊试液变红(1分)
(4)KMnO4溶液褪色(1分) 还原(1分)
(5)吸收SO2,防止污染环境。(2 分)
题目分析:(1)根据仪器的构造特点可知,盛装浓硫酸的仪器的名称是分液漏斗。
(2)装置连接好以后,必须检查装置的气密性。
(3)A中生成SO2,SO2具有漂白性,且溶于水生成亚硫酸,溶液显酸性,所以装置B、C中可观察到的实验现象分别品红溶液褪色、石蕊试液变红。
(4)SO2还具有还原性,能使酸性高锰酸钾溶液褪色,所以D中可观察到的现象是KMnO4溶液褪色。
(5)SO2是大气污染物,所以装置E的作用是吸收SO2,防止污染环境。2的制备、性质检验、尾气处理以及仪器的识别
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,注重基础知识的巩固与训练,侧重能力的培养。有助于培养学生规范、严谨的实验设计能力,提高学生的综合实验能力,提升学生的学科素养。该类试题重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。
