辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2)。一种以辉铜矿石为原料制备硝酸铜的工艺流程如下:
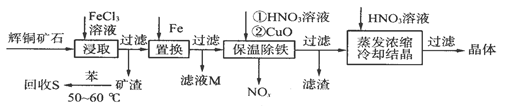
⑴写出浸取过程中Cu2S溶解的离子方程式:____________________。
⑵回收S过程中温度控制在50~60℃之间,不宜过高或过低的原因是_____________。
⑶气体NOx与氧气混合后通入水中能生成流程中可循环利用的一种物质,该反应的化学方程式为___________________________;向滤液M中加入(或通入)下列__________(填字母)物质,得到另一种可循环利用的物质。
a.铁 b.氯气 c.高锰酸钾
⑷保温除铁过程中,加入CuO的目的是________________________;蒸发浓缩时,要用HNO3溶液调节溶液的pH,其理由是___________________________。
(1)Cu2S+4Fe3+=2Cu2++4Fe2++S
(2)温度过高苯容易挥发,温度过低溶解速率小;
(3)4NOx+(5-2x)O2+2H2O= 4HNO3 b,(4)调节溶液的pH,使铁元素(Fe3+)完全转化为Fe(OH)3沉淀抑制Cu2+的水解(不引入其他杂质)
(1)Fe3+ 作氧化剂,Cu2S被氧化,离子议程式为:Cu2S+4Fe3+=2Cu2++4Fe2++S,答案:Cu2S+4Fe3+=2Cu2++4Fe2++S;(2)苯沸点比较低,温度过高苯容易挥发,从反应动力学来看,温度过低溶解速率小;答案:温度过高苯容易挥发,温度过低溶解速率小;(3)NOx作还原剂,根据质量守恒和电子得失写出方程式: 4NOx+(5-2x)O2+2H2O= 4HNO3;向滤液M中通入Cl2将FeCl2氧化成FeCl3,可循环使用,选b, 答案: 4NOx+(5-2x)O2+2H2O= 4HNO3;b;(4)Fe3++3H2O Fe(OH)3+3H+ ,加入CuO,使水解平衡正向进行,调节溶液的pH,使铁元素(Fe3+)完全转化为Fe(OH)3沉淀;加热过程中Cu2+ 会水解,加入硝酸抑制Cu2+的水解(不引入其他杂质);答案:调节溶液的pH,使铁元素(Fe3+)完全转化为Fe(OH)3沉淀 抑制Cu2+的水解(不引入其他杂质)
Fe(OH)3+3H+ ,加入CuO,使水解平衡正向进行,调节溶液的pH,使铁元素(Fe3+)完全转化为Fe(OH)3沉淀;加热过程中Cu2+ 会水解,加入硝酸抑制Cu2+的水解(不引入其他杂质);答案:调节溶液的pH,使铁元素(Fe3+)完全转化为Fe(OH)3沉淀 抑制Cu2+的水解(不引入其他杂质)
