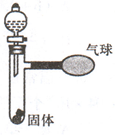
(4分)如下图所示,打开分液漏斗,使其中的无色液体与试管中的固体接触反应,可观察到气球胀大现象,请分别写出一个符合图中现象和下列要求的化学方程式:
(1) 分解反应:
(2) 化合反应:
(3) 复分解反应:
(4) 置换反应:
(1)2H2O2 2H2O+O2↑ (2)CaO+H2O==Ca(OH)2
2H2O+O2↑ (2)CaO+H2O==Ca(OH)2
(3)CaCO3+2HCl==CaCl2+H2O+C O2↑ (4)Zn+H2SO4==ZnSO4+H2↑
无色液体与试管中的固体接触反应,观察到气球胀大,可能是无色液体和固体发生化学反应生成了气体,导致气球胀大;也可能是固体物质与水反应放出大量的热,导致试管中的空气受热膨胀;据此结合四种基本的反应类型进行分析解答.
解:(1)过氧化氢溶液和二氧化锰固体混合能生成氧气,使气球胀大,该反应属于分解反应,反应的化学方程式为:2H2O2 2H2O+O2↑;
2H2O+O2↑;
(2)氧化钙与水反应放出大量的热,试管中的空气受热膨胀使气球胀大,该反应属于化合反应,反应的化学方程式为:CaO+H2O═Ca(OH)2;
(3)复分解反应是两种化合物相互交换成分生成另外两种化合物的反应,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳气体,使气球胀大,该反应属于复分解反应,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(4)置换反应是一种单质和一种化合物生成另一种单质和另一种化合物的反应,锌是固体单质,与稀硫酸反应生成氢气,使气球胀大,该反应属于置换反应,反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑.
故答案为:(1)2H2O2 2H2O+O2↑;(2)CaO+H2O═Ca(OH)2;
2H2O+O2↑;(2)CaO+H2O═Ca(OH)2;
(3)CaCO3+2HCl═CaCl2+H2O+CO2↑;(4)Zn+H2SO4═ZnSO4+H2↑.
本题有一定难度,理解气球胀大的原因(产生气体或与水反应放出热量)、掌握常见气体的制取及反应物的状态、氧化钙的化学性质等是正确解答本题的关键.
