工业上用活性炭吸附海带提碘后废水中的I-制取I2,其流程如下图:
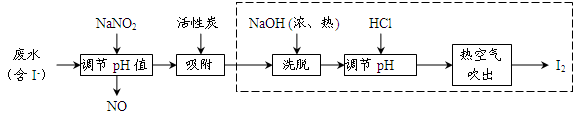
(1)向废水中加入NaNO2并调节pH<4,写出反应的离子方程式__________________。
(2)用活性炭吸附生成的单质碘的目的是__________________________,用浓、热NaOH洗脱吸附的碘的化学方程式为___________________________________。
(3)从调节pH后所得的溶液中获取碘,工业上可用热空气吹出,其原因是___________;若取少量该溶液在实验室中分离得到单质碘,需要进行的操作为__________________。
(4)流程中生成的NO尾气有毒,工业上将其与O2按一定比例通入NaOH制备NaNO2,写出反应的化学方程式:________________________________。
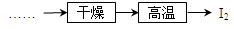
(5)工业上虚框内流程还可用如图操作代替,评价下图流程的优点___________________________(写出一条)。
(1)2NO2-+ 4H++ 2I- → 2NO + I2 + 2H2O (2分)
(2)富集单质碘(1分) 3I2 + 6NaOH → NaIO3+ 5NaI+ 3H2O(2分)
(3)单质碘在水中溶解度小,易升华(1分) 萃取 分液 蒸馏(3分)
(4)4NaOH+ O2+ 4NO → 4NaNO2+ 2H2O(2分)
(5)减少了化学药品的投入量,使成本大大降低。(或生产环节减少;或药品对设备无腐蚀性等)(1分,合理即可)
题目分析:(1)根据流程图信加入NaNO2时有NO生成,发生了氧化还原反应,故其离子方程式2NO2-+ 4H++ 2I- → 2NO + I2 + 2H2O。
(2)用活性炭吸附生成的单质碘的目的是富集单质碘。根据流程图最后加入酸时又有碘生成,可知用浓、热NaOH洗脱吸附的碘的化学方程式为3I2 + 6NaOH → NaIO3+ 5NaI+ 3H2O。
(3)从调节pH后所得的溶液中获取碘,工业上可用热空气吹出,其原因是单质碘在水中溶解度小,易升华;若取少量该溶液在实验室中分离得到单质碘先后进行的操作为 萃取、分液、蒸馏。
(4)根据氧化还原反应原理,反应的化学方程式4NaOH+ O2+ 4NO → 4NaNO2+ 2H2O。
(5)从能源的利用和环保方面思考做答,可以是减少了化学药品的投入量,使成本大大降低。(或生产环节减少;或药品对设备无腐蚀性等)
