(14分)
某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1)。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。
(1)请完成以下实验设计表(表中不要留空格):
| 编号 | 实验目的 | 碳粉/g | 铁粉/g | 醋酸/% |
| ① | 为以下实验作参照 | 0.5 | 2.0 | 90.0 |
| ② | 醋酸浓度的影响 | 0.5 | 36.0 | |
| ③ | 0.2 | 2.0 | 90.0 |
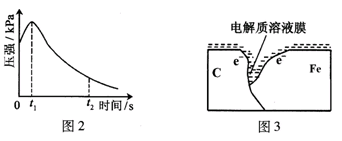
(3)该小组对图2中0~t1时压强变大的原因提出了如下假设,请你完成假设二:
假设一:发生析氢腐蚀产生了气体;
假设二: ;
……
(4)为验证假设一,某同学设计了检验收集的气体中是否含有H2的方案。请你再设计一个实验方案验证假设一,写出实验步骤和结论。
| 实验步骤和结论(不要求写具体操作过程): |
(1)②2.0 ③碳粉含量的影响
(2)吸氧腐蚀 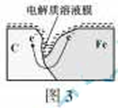 还原反应 2H2O+O2+4e-=4OH- (或4H++O2+4e-=2H2O)
还原反应 2H2O+O2+4e-=4OH- (或4H++O2+4e-=2H2O)
(3)反应放热,温度升高,体积膨胀
(4)实验步骤和结论(不要求写具体操作过程)
①药品用量和操作同编号①实验(多孔橡皮塞增加进、出导管)
②通入氩气排净瓶内空气;
③滴入醋酸溶液,同时测量瓶内压强变化(也可测温度变化,检验Fe2+等)。
如果瓶内压强增大,假设一成立。否则假设一不成立。
(本题属于开放性试题,合理答案均给分)
题目分析:(1)探究影响化学反应速率,每次只能改变一个变量,故有②中铁的量不变,为2.0g;③中改变了碳粉的质量,故为探究碳粉的量对速率的影响。
(2)压强与气体的物质的量成正比,从图中可以看出,气体的量开始增加,后减少,故为吸氧腐蚀;活泼金属做负极,故碳为正极,发生还原反应。
(3)从体积的影响因素着手,温度升高,体积增大
(4)基于假设一,可知,产生氢气,发送那些变化,从变化入手考虑
