问题
问答题
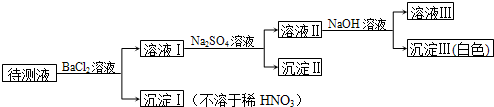
某待测液中可能含有Cu(NO3)2、Mg(NO3)2、AgNO3、Ba(NO3)2四种物质中的一种或几种,现进行如下图所示的实验(所加试剂均足量):
通过实验现象确定(用化学式表示):
(1)沉淀Ⅰ是______.
(2)原待测液中一定不含有______;可能含有______;
(3)写出生成沉淀Ⅲ的化学反应方程式:______.
答案
待测液加入氯化钡产生不溶于稀硝酸的白色沉淀,因此一定含有硝酸银;得到的溶液Ⅰ加入硫酸钠产生白色沉淀,说明溶液Ⅰ中含有钡离子,可能是加入的氯化钡溶液中的,也可能是待测液中含有硝酸钡;得到的溶液Ⅱ中加入氢氧化钠溶液产生白色沉淀,说明溶液中一定不含硝酸铜,一定含有硝酸镁,硝酸铜与氢氧化钠反应产生蓝色氢氧化铜沉淀,硝酸镁与氢氧化钠反应产生氢氧化镁沉淀.
(1)由上述分析可知沉淀Ⅰ为氯化银,化学式为AgCl
(2)溶液中一定不含硝酸铜,可能含有硝酸钡,化学式为Cu(NO3)2; Ba(NO3)2
(3)生成沉淀Ⅲ的反应是硝酸镁与氢氧化钠反应,化学方程式为:Mg(NO3)2+2NaOH=Mg(OH)2↓+2NaNO3
故答案为:(1)AgCl (2)Cu(NO3)2; Ba(NO3)2
(3)Mg(NO3)2+2NaOH=Mg(OH)2↓+2NaNO3
