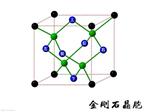
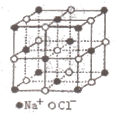
NaCl的晶胞如图所示,将NaCl晶胞中的所有Cl-去掉,并将Na+全部换成C原子,再在晶胞的4个“小立方体”中心处各放置一个C原子,且这四个“小立方体”互不共面,位于“小立方体”中的碳原子均与最近的4个碳原子成键,以此表示金刚石的一个晶胞。若再将在成键的C原子中心联线的中点处增添一个O原子,则构成了某种CO2的晶胞。则下面说法正确的是( )(已知C-C键的键长1.54×10-10m)
A.一个金刚石的晶胞中有8个C原子
B.金刚石的密度为3.54g·cm-1
C.在该种CO2晶体中,一个CO2分子由一个C原子和二个氧原子构成
D.在该种CO2晶胞中含氧原子8个
AB
题目分析:根据题意,给出金刚石晶胞,如右图:金刚石晶胞中C原子数为4.;计算方式是8个黑色的一共是1个C,6个蓝色的一共是3个C,加起来是4 个。绿色的在晶胞里面,应该有4个C,加起来有8个。A正确;体对角线的1/4是C-C键长,体对角线是0.154×4=0.616nm,正方体体对角线是正方体边长的√3倍,因此,正方体边长=0.616/√3=0.356nm, 1mol金刚石质量12g,,含6.02×1023个C原子,一个金刚石晶胞体积是(0.356 × 10-7)3立方厘米,而每个晶胞内含8个C原子,所以共有(6.02×1023)/8个晶胞,因而12g金刚石的总体积是(6.02×1023)/8×[0.356×10-7]3立方厘米,两者相除就得出密度,是3.503g·cm-3。B正确。C.在该种CO2晶体中,无CO2分子,C错误;D.在该种CO2晶胞中含氧原子16个,D错误。