Ⅰ.某同学欲测定硫酸铜晶体中结晶水的含量。他列出的实验用品为:硫酸铜晶体试样、研钵、坩埚、坩埚钳、酒精灯、三脚架、玻璃棒、药匙、托盘天平。回答下面问题:
(1)完成本实验还需要的实验用品有_________。
(2)下面的情况有可能造成测定结果偏低的是_________ (填序号) 。
A.试样中含有易挥发的杂质
B.加热时有晶体溅出
C.晶体加热脱水不完全
D.实验前坩埚未完全干燥
E.硫酸铜受热分解
Ⅱ.该同学发现硫酸铜晶体加热后变黑,查阅资料得知: 硫酸铜在加热条件下生成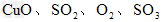 。现用下图所示的装置验证硫酸铜在加热分解时有SO2产生,并测量产生的O2的体积。试填写下列空白:
。现用下图所示的装置验证硫酸铜在加热分解时有SO2产生,并测量产生的O2的体积。试填写下列空白:
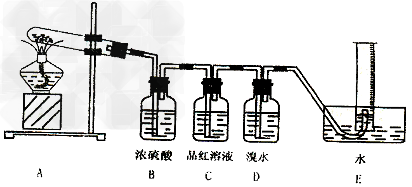
(3)硫酸铜受热分解的化学方程式为_________。
(4)装置B的作用是_________ ,装置D的作用是_________。
(5)停止加热时,测量收集到的气体体积必须包括以下几步:
①__________________;
②调整量筒内外液面高度使之相同;
③读取量筒内气体的体积。
(6)测量收集到的气体体积时,如何使量筒内外液面的高度相同? __________________。
(7)Y为ⅥA族元素构成的气态单质,将Y和SO2分别通入品红溶液,都能使品红溶液褪色。则Y的化学式为_________;简述区别二者的实验方法__________________。
(1)泥三角、干燥器
(2) C
(3)
(4)吸收反应后的三氧化硫气体;除尽二氧化硫
(5)使试管和量筒内的气体都冷却至室温
(6)慢慢将量筒下移
(5)O3;加热褪色后的溶液,若溶液恢复红色,则原通入气体为SO2,否则为O3。
