问题
实验题
某校化学兴趣小组设计了如图示实验装置(图中省略了夹持仪器)来测定某铁碳合金中铁的质量分数。
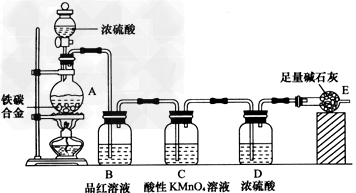
(1)mg铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A、B 均无明显现象,其原因是①常温下碳与浓硫酸不反应;②____________________
(2)写出加热时A中碳与浓硫酸发生反应的化学方程式:_________________
(3)B中的现象是____________;C的作用是__________
(4)待A中不再逸出气体时,停止加热,拆下E并称重,E增重 bg。则铁碳合金中铁的质量分数为____________。
(5)甲同学认为利用此装置测得铁的质量分数偏大,请你写出可能的原因:__________。
(6)最后对所得测量结果进行评价,小组内有同学提出,本套装置在设计上存在多处缺陷而导致实验结果不准确,其中会导致铁的质量分数测量值偏低的是__________________(任答一条即可)。
答案
(1)常温下Fe遇浓硫酸发生钝化
(2)C+2H2SO4(浓)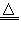 CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
(3)品红溶液褪色;除尽反应产物中的SO2气体
(4)(11m-3b)/11m
(5)装置内的CO2难以赶尽,导致E的质量增重偏小
(6)SO2不一定能全部被品红溶液、酸性KMnO4溶液除去(或E中碱石灰会吸收空气中的CO2、H2O,其他合理答案即可)
