石灰石的主要成份是碳酸钙,此外还有 SiO2 、 Fe2O3、 Al2O3等杂质。测定石灰石中钙元素的质量百分含量的流程图如下:
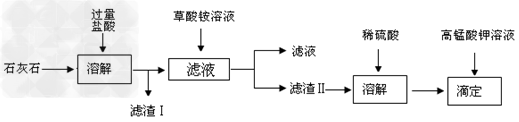
已知:草酸(H2C2O4)是一种二元弱酸。
(1)滤渣Ⅰ的成分是_________,该物质溶于氢氧化钠溶液的化学方程式为__________________________。
(2)请写出生成滤渣Ⅱ(CaC2O4·H2O)的离子方程式____________________。
(3)加入的(NH4)2C2O4 溶液要求是饱和的,其原因是____________。不仅如此,在加入饱和(NH4)2C2O4 溶液后,还需要向溶液中滴加氨水,其原因是_______________ 。
(4)将草酸钙沉淀 (CaC2O4·H2O),用硫酸溶解,用a mol/L的标准高锰酸钾溶液滴定生成的草酸,发生化学反应:H2C2O4 + MnO4- + H+ → Mn2+ + CO2 ↑+ H2O(未配平),其中还原剂是___________。若开始取用样品的质量为m g,硫酸溶解后所得草酸溶液的体积为100mL,每次取25.00mL进行滴定,达到滴定终点时所耗KMnO4溶液体积为 b ml(三次平均值),所得草酸溶液的物质的量的浓度是____________ ;石灰石中钙元素的质量百分含量为_________。(相对原子质量:Ca-40)
(1)SiO2;SiO2 + 2NaOH = Na2SiO3 + H2O
(2)C2O42-+Ca2++H2O=CaC2O4·H2O↓
(3)保持较大的C2O42-离子浓度,使Ca2+沉淀完全;中和过量的盐酸,使溶液中 C2O42-浓度慢慢增大,可以生成CaC2O4沉淀
(4)H2C2O4;0.1ab mol/L;0.4ab/m×100%