硼(B)、铝(Al)、镓(Ga)均属于硼族元素(第ⅢA族),它们的化合物或单质
都有重要用途。回答下列问题:
(1)写出基态镓原子的电子排布式 。
(2)已知:无水氯化铝在178℃升华,它的蒸气是缔合的双分于(Al2Cl6),更
高温度下Al2Cl6则离解生成A1Cl3单分子。
①固体氯化铝的晶体类型是 ;
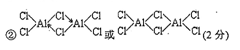
②写出Al2Cl6分子的结构式 ;
 ③单分子A1Cl3的立体构型是 ,缔合双分子Al2Cl6中Al原子的轨道杂化类型是 。
③单分子A1Cl3的立体构型是 ,缔合双分子Al2Cl6中Al原子的轨道杂化类型是 。
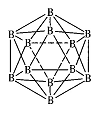
(3)晶体硼的结构单元是正二十面体,每个单元中有12个硼原予(如图)
其中有两个原子为10 B,其余为11B,则该结构单元有 种不同的结构
类型。
(4)金属铝属立方晶系,其晶胞边长为405 pm,密度是2.70g·cm-3,计算确
定其晶胞的类型(简单、体心或面心立方) ;晶胞中距离最近的铝原
子可看作是接触的,列式计算铝的原子半径r(A1)= pm。
(1)1s2 2s22p6 3s2 3p6 3d10 4s2 4p1 或〔Ar〕3d10 4s2 4p1
(2)①分子晶体
②
③ 平面三角形 sp3
(3)3
(4)N(Al)×27/4053×10-30×6.02×1023=2.70,解得N(Al)=4.00,为面心立方晶胞
×405pm/4=143pm.
(1)镓是31号元素,其原子核外有31个电子,根据构造原理知其核外电子排
布式1s2 2s22p6 3s2 3p6 3d10 4s2 4p1 或〔Ar〕3d10 4s2 4p1
(2)①分子晶体的熔沸点较低,氯化铝的熔沸点较低,所以为分子晶体。
②铝原子和氯原子之间形成共价键,还形成一个配位键,其结构为
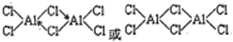 。
。
③氯化铝中每个铝原子含有3个共价键,且不含孤电子对,为平面三角形结构,
缔合双分子Al2Cl6中Al原子的轨道杂化类型sp3。
(3)两个10B相邻、相间、相对,所以共有3种类型结构。
(4)每个晶胞中含有铝原子个数=ρV/M/NA=2.70×(405×10−10)3/17/NA==4.00,
该晶胞的每个顶点上和每个面上都含有一个Al原子,为面心立方晶胞,面心立
方晶胞中,每个面的对角线上三个原子紧挨着,所以对角线长度=21/2×405pm/4
=143pm。
