由Fe2O3、CuO、A1、C中的几种物质组成的混合粉末,取样品进行下列实验(部分产物略去):
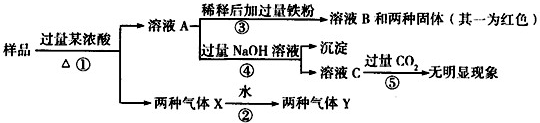
(1)混合气体Y中两种气体的化学式是______,反应①中生成混合气体X的化学方程式是______.
(2)通过上述实验及其现象说明,一定不含有的物质是______,不能确定是否含有的物质是______;
(3)为进一步确定样品中的未知物质,可以用上述反应过程中的溶液,设计一个简单的后续实验就可以确定,方法是:
______.
(1)气体X与水反应得Y为两种气体的混合物,则其中一种为NO2,气体Z为NO、CO2混合物,则浓酸为浓硝酸.
反应①中生成混合气体X的化学方程式为C+4HNO3(浓)=CO2↑+4NO2↑+2H2O.
故答案为:NO、CO2;C+4HNO3(浓)=CO2↑+4NO2↑+2H2O.
(2)无论加什么浓酸(硫酸和硝酸),溶液A中都可能含有Fe3+、Cu2+、Al3+三种金属阳离子.向溶液A中加入过量的NaOH溶液,可转化为Fe(OH)3和Cu(OH)2沉淀析出,如果有Al3+,则可转化为ALO2-离子,溶液C通入CO2后,会发生反应产生白色沉淀Al(OH)3.
向溶液A中加过量Fe粉,得B溶液和两种固体,且一种固体为红色(Cu),另一种就是过量的Fe粉.
根据上述分析可知,样品中一定没有Al,一定有CuO和C,不能确定是否有Fe2O3.
故答案为:A1; Fe2O3.
(3)不能确定是否有Fe2O3,若有则溶液A中含有Fe3+,用KSCN溶液检验溶液A中是否含有Fe3+.方法是取溶液A少许,向其中加入KSCN溶液,若溶液变红色,说明样品中含有Fe2O3;若溶液不变红色,说明样品中没有Fe2O3.
故答案为:取溶液A少许,向其中加入KSCN溶液,若溶液变红色,说明样品中含有Fe2O3;若溶液不变红色,说明样品中没有Fe2O3.
