某白色固体可能是Na2SO3、Na2SO4、Na2CO3中的两种或三种,化学兴趣小组在实验室对该固体进行探究:取少量固体滴加稀硫酸并将产生的气体通入澄清的石灰水后出现浑浊.一位同学由此得出该固体一定含有Na2CO3的结论.
(1)请指出该结论是否合理并说明理由______.
(2)请完成对该固体的探究:
①提出合理假设
假设1:______;假设2:______;假设3:______.
假设4:含有Na2SO3、Na2SO4和Na2CO3
②基于假设,设计出实验方案,在答题卷中画出装置图并描述实验操作、预期的实验现象和结论.
(1)因为若固体是Na2SO3和Na2SO4滴加稀硫酸并将产生的气体通入澄清的石灰水后也会出现浑浊,
SO2+Ca(OH)2=CaSO3↓+H2O,所以该同学分析不合理;
故答案为:不合理 因为若固体是Na2SO3和Na2SO4滴加稀硫酸并将产生的气体通入澄清的石灰水后也会出现浑浊;
(2)①依据白色固体可能是Na2SO3、Na2SO4、Na2CO3中的两种或三种,结合假设4:含有Na2SO3、Na2SO4和Na2CO3,所以固体由两种物质的可能组成为:固体含有Na2SO3、Na2SO4;固体含有Na2SO3、Na2CO3;固体含有Na2SO4、Na2CO3;
故答案为:假设1:固体含有Na2SO3、Na2SO4;假设2;固体含有Na2SO3、Na2CO3;假设 3;固体含有Na2SO4、Na2CO3;
②根据假设继续实验设计的主要依据是,根据生成的气体性质进行验证、检验、分析、判断.由于二氧化硫和二氧化碳气体都和澄清石灰水反应生成沉淀变浑浊,所以在设计实验时,要考虑怎样验证二氧化硫气体,怎样验证二氧化碳气体,如何避免二氧化硫气体对二氧化碳气体检验的干扰,是解决本题的关键,所以设计思路为先用品红验证二氧化硫的存在,再用高锰酸钾溶液除去二氧化硫,用品红验证二氧化硫是否除净,最后通入澄清石灰水检验纯净的二氧化碳气体的存在,最后进行尾气的吸收;设计实验装置图和试剂如图所示:
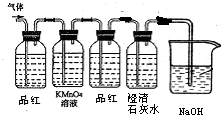
取少量固体滴加足量稀盐酸并将产生的气体通过上述装置,若看到第一个洗瓶的溶液腿色说明有Na2SO3,若第三个洗瓶的溶液颜色没有变化且第四个洗瓶中出现浑浊说明有Na2CO3;在与稀盐酸反应完的溶液中滴入BaCl2溶液若产生沉淀说明有Na2SO4;若第一个瓶褪色,第四个瓶变浑浊,反应液中加入BaCl2溶液产生沉淀,说明固体符合假设4;若第一个瓶褪色,第四个瓶无变化,反应液中加入BaCl2溶液产生沉淀,说明假设1符合;若第一个瓶无变化,第四个瓶变浑浊,反应液中加入BaCl2溶液产生沉淀,说明假设3符合;若第一个瓶褪色,第四个瓶变浑浊,反应液中加入BaCl2溶液无沉淀,则说明假设2符合;
故答案:

取少量固体滴加足量稀盐酸并将产生的气体通过上述装置,若看到第一个洗瓶的溶液腿色说明有Na2SO3,若第三个洗瓶的溶液颜色没有变化且第四个洗瓶中出现浑浊说明有Na2CO3;在与稀盐酸反应完的溶液中滴入BaCl2溶液若产生沉淀说明有Na2SO4;若第一个瓶褪色,第四个瓶变浑浊,反应液中加入BaCl2溶液产生沉淀,说明固体符合假设4;若第一个瓶褪色,第四个瓶无变化,反应液中加入BaCl2溶液产生沉淀,说明假设1符合;若第一个瓶无变化,第四个瓶变浑浊,反应液中加入BaCl2溶液产生沉淀,说明假设3符合;若第一个瓶褪色,第四个瓶变浑浊,反应液中加入BaCl2溶液无沉淀,则说明假设2符合;