某混合金属粉末,除Mg外,还含有Al、Zn中的一种或两种,含量都在10%以上.某研究小组设计实验探究该混合金属粉末中铝、锌元素的存在.所用试剂:样品、pH试纸、稀H2SO4、NaOH溶液、稀NH3•H2O.该小组探究过程如下:
●查阅资料:
| ①镁、铝、锌都是银白色的金属 ②锌(Zn)可以与NaOH溶液反应生成H2 ③Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3•H2O ④Zn2+易形成络合物如[Zn(NH3)4]2+,该络合物遇强酸分解生成Zn2+、NH4+ |
(1)假设①:该混合金属粉末中除镁外还含有______元素
假设②:该混合金属粉末中除镁外还含有______元素
假设③:该混合金属粉末中除镁外还含有铝、锌元素
●实验探究:
甲同学基于假设③设计实验方案如下:乙同学同样基于假设③设计另一实验方案如下:
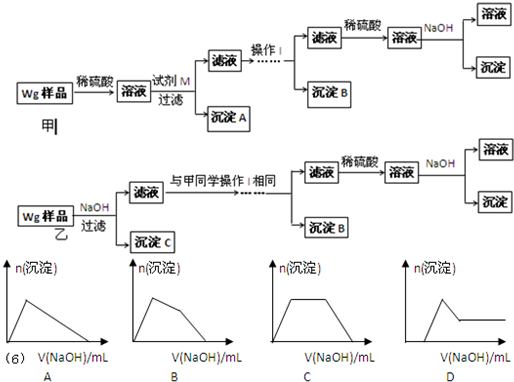
(2)试剂M是______;沉淀B是______.
(3)丙同学认为乙同学的方案比甲同学的好,理由是______.
(4)丁同学研究了甲、乙两同学的方案后,在其中一种方案的基础上用最简便方法测定了Wg样品中金属镁(Mg)的质量,他的方法是______.
(5)操作Ⅰ的主要过程是:在滤液中逐滴加入______,直至生成的沉淀刚好溶解,再加入足量的______.
(6)某溶液中含有Zn2+、Al3+、NH4+和SO42-等离子,向其中逐滴加入NaOH溶液,则生成沉淀的物质的量与加入NaOH溶液体积关系的图象正确的是______.
(1)除Mg外,还含有Al、Zn中的一种或两种,因此粉末的组成有三种可能,即除Mg外只含Al、只含Zn、或既含Al又含Zn,故答案为:Al;Zn;
(2)由实验方案可知镁盐、铝盐和锌盐形成的沉淀分三次分离,第一次为:Mg(OH)2,试剂M为NaOH溶液,第二次为:Al(OH)3,铝盐和锌盐加过量的强碱先生成了沉淀,然后沉淀溶解,在滤液中逐滴加入稀硫酸,直至生成的沉淀刚好溶解又形成了铝盐和锌盐,锌盐加过量的弱碱先生成了沉淀,然后沉淀溶解,铝盐加过量的弱碱也生成了沉淀,然后沉淀不溶解,实现了Al(OH)3沉淀的分离;第三次为Zn(OH)2,在滤液中逐滴加入稀硫酸,直至生成的沉淀刚好溶解,再加入适量的NaOH溶液,形成沉淀,故答案为:NaOH溶液;Al(OH)3;
(3)对比甲、乙两同学的实验,发现甲比乙多了第一步加稀硫酸,故答案为:步骤简单,节约试剂;
(4)锌、铝都能与NaOH溶液反应溶解,而镁不能与NaOH溶液反应,所以只需将沉淀C洗涤、小心干燥后称量即可得到镁的质量,故答案为:将沉淀C洗涤、小心干燥后称量;
(5)铝盐和锌盐加过量的强碱先生成了沉淀,然后沉淀溶解,在滤液中逐滴加入稀硫酸,直至生成的沉淀刚好溶解,又形成了铝盐和锌盐,锌盐加过量的弱碱先生成了沉淀,然后沉淀溶解,铝盐加过量的弱碱也生成了沉淀,然后沉淀不溶解,这样实现了Al(OH)3沉淀的分离,故答案为:稀硫酸;稀氨水;
(6)先发生的反应是Al3+和Zn2+与OH-生成沉淀,随后随着NaOH的加入,沉淀减少直至消失,此时是因为生成的沉淀都能溶解在NaOH溶液中,但Al(OH)3~NaOH,Zn(OH)2~2NaOH,所以相同物质的量的沉淀溶解消耗的NaOH不同,最后NH4+和OH-反应生成NH3•H2O,故选:B.
