问题
问答题
2.5g固体氧化物X,经过以下两步反应后,得到2g红色固体单质C.
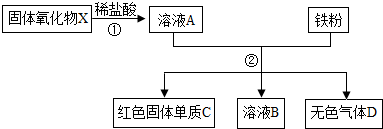
上述第②步恰好反应完全,溶液B只含一种溶质,且是盐.
(1)第①步盐酸是否过量?判断根据是什么?______
(2)X是______(填写化学式).
答案
(1)铁粉与①加盐酸后所得的溶液A反应能生成无色气体D,说明是铁与酸反应得到氢气,所以①步盐酸过量;(2)固体氧化物与盐酸反应能生成金属氯化物,属于盐类物质,与铁反应生成了亮红色的固体单质C,该单质为铜,根据质量守恒定律,说明原固体氧化物中含铜,故固体氧化物X为氧化铜,化学式是CuO.
故答为:
(1)过量,加入铁粉后有无色气体D放出;
(2)CuO.
