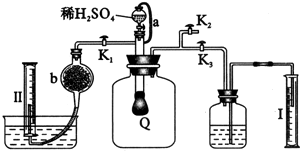
为测定已变质的过氧化钠的纯度,设计如下图所示的实验;Q为一具有良好的弹性气球,称取一定量的样品放于其中,按图安装的实验装置打开分液漏斗的活塞,将稀H2SO4滴入气球中.请填空:
(1)Q内发生反应生成______种气体,其中的反应有______个氧化还原反应.
(2)为测定反应生成气体的总体积,滴稀H2SO4前必须关闭(填K1、K2或K3,下同)______,打开______.
(3)当上述反应停止,将K1、K2、K3处于关闭状态,然后先打开K2,再缓缓打开K1,这时可观察到的现象是______.
(4)导管a的作用是______.
(5)b中装的固体试剂是______,为何要缓缓打开K1______.
(6)实验结束时量筒I中有x mL水,量筒II中收集到y mL气体,则过氧化钠的纯度是______(体积折算到标准状况).
(1)变质的过氧化钠中含有碳酸钠,加入酸后Q内发生反应:2Na2O2+2H2SO4=2Na2SO4+2H2O+O2↑;Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,前者的氧元素的化合价发生了变化,是氧化还原反应,后者元素的化合价未变,是非氧化还原反应,故答案为:2;1;
(2)反应产生的CO2、O2使气球变大,将广口瓶中气体排出,水进入量筒Ⅰ中,所以量筒Ⅰ中水的体积即为产生的CO2、O2的体积,所以滴稀H2SO4前必须关闭K1、K2打开K3,
故答案为:K1、K2;K3;
(3)反应停止,打开K2,再缓缓打开K1,广口瓶内外相通,气球Q慢慢缩小,故答案为:气球Q慢慢缩小;
(4)为使分液漏斗内液体顺利流下,应是分液漏斗内外压强相等,所以导管a的作用是平衡分液漏斗上下的压强使顺利流下,故答案为:平衡分液漏斗上下的压强使顺利流下;
(5)混合气体通过碱石灰吸收CO2,最后量筒Ⅱ中收集的是O2,故答案为:碱石灰;控制气体流速,使CO2充分吸收;
(6)2Na2O2+2H2SO4=2Na2SO4+2H2O+O2↑; Na2CO3 +H2SO4=Na2SO4+H2O+CO2↑,
×2 y×10 -3 22.4 y×10 -3 22.4 (x-y)×10 -3 22.4 (x-y)×10 -3 22.4
则过氧化钠的质量为:
×2×78,碳酸钠的质量为:y×10 -3 22.4
×106, (x-y)×10 -3 22.4
所以过氧化钠的纯度:
=m(过氧化钠) m(过氧化钠)+m(碳酸钠)
,故答案为:78y 53x+25y
.78y 53x+25y
