某无色溶液X,由K+、NH+4、Ba2+、Al3+、Fe3+、CO2-3、SO2-4中的若干种离子组成,取该溶液进行如图实验: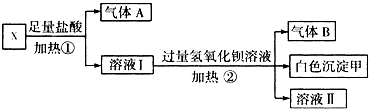
(1)白色沉淀甲是______;
(2)试写出实验过程中生成气体A、B的离子方程式______、______;
(3)通过上述实验,可确定X溶液中一定存在的离子是______,尚未确定是否存在的离子是______.
无色溶液,判断Fe3+不存在,加过量盐酸生成气体和溶液,判断溶液中一定含CO32-;则一定不含有Ba2+、Al3+;气体A为CO2;溶液I加入过量氢氧化钡反应生成气体B为氨气,一定有铵根离子,白色沉淀甲是硫酸钡,原溶液一定含有硫酸根.
(1)白色沉淀甲是硫酸钡,故答案为:硫酸钡;
(2)碳酸钠溶液与过量稀盐酸混合完全反应生成CO2,反应的离子方程式为CO32-+2H+=H2O+CO2↑,铵盐能与碱反应生成氨气:NH+4+OH-=NH3↑+H2O,故答案为:CO32-+2H+=H2O+CO2↑;NH+4+OH-=NH3↑+H2O;
(3)X溶液中一定存在的离子是CO32-、SO2-4,一定不存在的离子是Fe3+、Ba2+、Al3+,尚未确定是否存在的离子是K+,故答案为:CO32-、SO2-4;K+;
