有一包固体A,可能含有CuO、Cu、NaOH、Na2CO3、Ca(OH)2中的几种,取少量的A做如下实验进行探究.试根据实验过程中的现象判断:
(1)气体D是______,沉淀G是______.
(2)写出过程②中一定发生的化学方程式______.
(3)写出过程③发生的化学方程式______.
(4)原固体混合物A中一定含有的物质______.
(5)滤液B中,还可能存在的溶质是______,若要证明该物质是否存在,应该补做的实验是(写出主要的实验步骤、现象及结论)______.
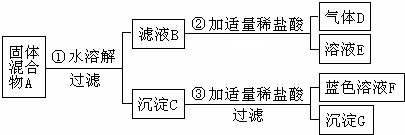
(1)得到的滤液B能与盐酸反应生成气体D,则滤液B中含有碳酸钠,生成的D为二氧化碳,得到的沉淀C能与盐酸反应生成蓝色溶液F,则F为氯化铜,由盐酸与氧化铜反应生成,铜不与盐酸反应,故沉淀G为铜,碳酸钙能与盐酸反应生成二氧化碳气体,沉淀C与盐酸反应无气体产生,故C中不含有碳酸钙,混合物A中不含有氢氧化钙,所以本题答案为:二氧化碳,铜;
(2)加入盐酸产生了二氧化碳,则碳酸钠与盐酸反应生成了氯化钠、二氧化碳和水,所以本题答案为:Na2CO3+2HCl═2NaCl+CO2↑+H2O;
(3)氧化铜能与盐酸反应生成氯化铜和水,所以本题答案为:CuO+2HCl═CuCl2+H2O;
(4)根据推断,原物质中一定含有碳酸纳、氧化铜和铜,所以本题答案为:碳酸纳、氧化铜和铜;
(5)滤液B中还可能含有氢氧化钠,要证明其存在,可以将碳酸钠除去,加入酚酞试液观察是否变红进行判断,所以本题答案为:氢氧化钠,取样品少许,放入试管中,加入水溶解,然后向溶液中加入过量的氯化钙溶液,然后向上层清液加入酚酞试液,若试液变红,则含有氢氧化钠.
