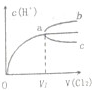
室温下,将Cl2缓慢通入水中.当通入的Cl2体积为V1时达到饱和(假设Cl2在水中只发生如下反应:Cl2+H2O=HCl+HClO,溶液中c(H+)变化入下图中的曲线a.已知Cl2的溶解度随温度的升高而迅速降低,下列叙述中正确的( )
A.在饱和氯水中加入NaOH使Ph>7,所得溶液存在下列关系:c(Na+)+c(H+)=c(Cl-)+C(OH-)+c(ClO-)
B.将饱和氯水升高温度,溶液中C(H+)的变化如曲线c
C.将饱和氯水加水稀释,溶液中C(H+)的变化如曲线b
D.在饱和氯水中加入NaOH使Ph=7,所得溶液存在下列关系:c(Na+)>c(CIO-)>c(Cl-)>c(HClO)
A、任何溶液都满足电中性,在饱和氯水中加入NaOH使pH>7,溶液中存在下列关系:c(Na+)+c(H+)=c(Cl-)+c(OH-)+c(ClO-),故A正确;
B、Cl2的溶解度随温度的升高而迅速降低,升高温度,氯气的浓度减小,平衡向左移动,溶液中c(H+)降低,变化如曲线c,故B正确;
C、饱和氯水浓度很小,加水稀释促进次氯酸的电离,氢离子的物质的量增多,但体积增大,氢离子浓度反而减小,故C错误;
D、溶液PH=7时,次氯酸过量,溶液中存在:c(Cl-)=c(HClO)+c(ClO-),c(Cl-)>c(ClO-),故D错误;
故选AB.
