问题
填空题
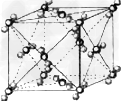
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F。其中B、D、F原子最外电子层的p能级(轨道)上的电子处于半满状态。通常情况下,A的一种氧化物分子为非极性分子,其晶胞结构如下图所示。E的电负性在该周期中最大。镓(Ga)与元素B形成的一种化合物是继以C单质为代表的第一代半导体材料和GaF为代表的第二代半导体材料之后,在近10年迅速发展起来的第三代新型半导体材料。
试回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)
(1)基态Ga原子的核外电子排布式为________________。
(2)A、B、C的第一电离能由大到小的顺序为________。
(3)B元素的单质分子中有______个π键。
(4)上述A的氧化物分子中心原子采取______杂化,其晶胞中微粒间的作用力为______
(5)FH3沸点与比BH3_____(填“高”或“低”),原因是________________。
(6)当0.01摩尔CrE3·6H2O在水溶液中用过量的AgNO3溶液处理时,常产生0.02摩尔的AgE沉淀,已知配离子配位数为6,此样品中配离子最可能是_______________。
答案
(1)1s22s22p63s23p63d104s24p1
(2)N>C>Si
(3)2
(4)sp;范德华力
(5)低;NH3分子间能形成氢键,而AsH3分子间不能形成氢键
(6)[Cr(H2O)5Cl]2+
