问题
问答题
(1)请写出Cr原子基态的电子排布式:______.
(2)H3O+的空间构型是______,其中O原子呈______杂化.
(3)Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于______晶体.
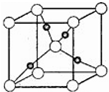
(4)某铜的氧化物晶体的晶胞结构如图所示,其中小球表示Cu原子,在1个晶胞所包含的氧原子数目为______.
答案
(1)Cr的原子序数为24,根据能量最低原理和洪特规则可写出电子排布式为1s22s22p23s23p23d54s1,
故答案为:1s22s22p23s23p23d54s1;
(2)H3O+中含有3个δ键和1个孤电子对,分子的立体构型为三角锥形,O原子呈sp3杂化,
故答案为:三角锥形;sp3;
(3)Fe(CO)5常温下呈液态,熔沸点较低,易溶于非极性溶剂,应为分子晶体,故答案为:分子;
(4)O原子位于晶胞的顶点和体心,晶胞中共含有O原子个数为:8×
+1=2,1 8
故答案为:2.
