(8分)物质丙是重要的化工产品,在国民经济中占有重要地位。工业上用甲和乙在高温高压加催化剂的条件下合成丙。甲、乙、丙的微观示意图见下表。
| 物质 | 甲 | 乙 | 丙 |  |
| 微观示意图 |  | 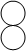 |  |
(2)甲、乙、丙中属于化合物的是(填序号) 。
(3)已知物质丙中氢元素的化合价为+1,则另一种元素的化合价为 。
(4)写出甲和乙合成丙反应的化学方程式 。
(5)现用10g的甲和60g的乙混合反应制取丙,反应一段时间后,经测定剩余甲的质量为4g,则剩余乙的质量为 g。
(6)在生产丙的原料中,甲是用水与碳高温反应(将水蒸汽通过高温碳层,这种方法又称为水煤汽法)制得的,这个过程还生成另一种产物一氧化碳;请你根据信息写出该反应的化学方程式 。
(1)分子 (2)丙 (3)-3 (4)N2+3H2 催化剂 2NH3
(5)32 (6) H2O+C高温H2+CO
题目分析:根据微观示意图可知:甲是H2,乙是N2,丙是NH3。
(1)甲物质的粒子是由2个H原子构成的氢分子,乙物质的粒子是由两个N原子构成的氮分子,丙物质的粒子是由一个N原子和3个氢原子构成的氨分子,这三种物质都是由分子构成的;
(2)甲物质的分子由同种原子H原子构成的、乙物质的分子由同种原子N原子构成的,均为单质的分子;而丙物质的分子由1个N原子、3个H原子,两种不同种原子构成的,该分子为化合物分子,因此,物质丙为化合物;
(3)物质丙的化学式为NH3,其中氢为+1价,根据正负化合价代数和为0的原则,N的化合价为-3价;
(4)根据题意可知,氢气和氮气反应生成氨气,故该反应的化学方程式为N2+3H2催化剂2NH3;
(5)由题意知参加反应的甲的质量为10g-4g=6g,设参加反应的乙的质量为x,则
N2+3H2催化剂2NH3
28 6
X 6g
28:6 = x:6g
解得,x=28g
则剩余的乙的质量为60g-28g=32g
(6)根据题意可知,水与碳在高温下反应,生成氢气和一氧化碳,故该反应的化学方程式为H2O+C高温H2+CO
点评:分子是由原子构成的,且同种原子构成的分子是单质分子,不同种原子构成的分子是化合物分子。试题通过给出微粒的模型,考查学生的观察能力和对基本概念的理解与运用能力,以检测考生从微观角度认识化学的意识和能力。
