问题
填空题
实验室要用12mol/L的浓盐酸配制1.0mol/L的稀盐酸91mL.
(1)要配制上述溶液,需用______量取12mol/L的浓盐酸______mL.
(2)配制过程中,除(1)中所选仪器、以及烧杯、玻璃棒、胶头滴管外,还需用到的仪器有______.
(3)A、B是配制溶液时可能用到的二种仪器的一部分,请根据提供的情景按要求回答问题.
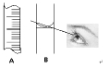
①写二种仪器的名称A______;B______.
②若按B中视线观察液面,则还需要继续进行的操作是______;
此操作完毕时,配制溶液的浓度______(填偏高、偏低、相符).
答案
(1)没有91mL容量瓶,故选择100mL容量瓶,根据稀释定律,稀释前后溶质HCl的物质的量不变,令需要浓盐酸的体积为V,则:V×12mol/L=1.0mol/L×100mL,解得V=8.3mL,故选择规格为10mL量筒,故答案为:10mL量筒,8.3;
(2)用用12mol/L的浓盐酸配制1.0mol/L的稀盐酸91mL,用量筒量取浓盐酸,在烧杯中稀释,并用玻璃棒搅拌,冷却后用玻璃棒引流移入10mL容量瓶中,洗涤并将洗涤液移入容量瓶,加水至刻度线1-2cm时,改用胶头滴管滴加至刻度线,盖好瓶塞摇匀,需要的仪器为:量筒、烧杯、玻璃棒、100mL容量瓶、胶头滴管等,缺少的仪器为:100mL容量瓶,
故答案为:100mL容量瓶;
(3)①A、B是配制溶液时可能用到的二种仪器的一部分,A含有刻度线,故A为量筒,B只有刻度线,B为容量瓶,
故答案为:量筒,容量瓶;
②图中为定容时仰视液面,液面应在刻度线上方,故需要用胶头滴管滴加蒸馏水直到与容量瓶刻线相切,所配溶液的体积偏大,故溶液浓度偏低,
故答案为:用胶头滴管滴加蒸馏水直到与容量瓶刻线相切,偏低.
