问题
选择题
高温下,某反应达到平衡,平衡常数K=
.恒容时,温度升高,H2浓度减小.下列说法正确的是( )c(CO)•c(H2O) c(CO2)•c(H2)
A.升高温度,逆反应速率减小
B.该反应的焓变为正值
C.恒温恒容下,增大压强,H2浓度一定减小
D.该反应的化学方程式为CO+H2O 催化剂 高温 CO2+H2
答案
平衡常数k=
,所以该反应化学方程式应为CO2+H2c(CO)•c(H2O) c(CO2)•c(H2)
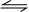
CO+H2O.
A、温度升高,正逆反应都增大,故A错误;
B、恒容时,温度升高,H2浓度减小,平衡向正反应移动,升高温度平衡向吸热反应移动,故正反应为吸热反应,即该反应的焓变为正值,故B正确;
C、恒温恒容下,增大压强,如果是加入稀有气体的话,各物质浓度没有变,所以平衡不移动,此时各物质的浓度不会变化,若增大二氧化碳浓度,H2浓度一定减小,若中等CO或水的浓度,H2浓度一定增大,故C错误;
D、平衡常数k=
,所以该反应化学方程式应为CO2+H2c(CO)•c(H2O) c(CO2)•c(H2)
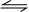
CO+H2O,故D错误.
故选B.
