补铁剂中铁元素的含量是质检部门衡量其质量的重要指标,实验主要包括如下步骤:
①配制0.01mol•L-1、0.008mol•L-1等一系列浓度的[Fe(SCN)6]3-(红色)标准比色液
②样品处理
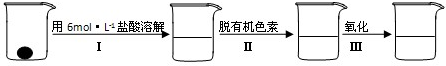
③准确量取一定体积的待测液于比色管中,加入稍过量的KSCN溶液,并稀释到10mL
④比色,直到与选取的标准颜色一致或相近即可.
试回答下列问题:
(1)配制25mL0.01mol•L-1标准溶液,需要的玻璃仪器有:烧杯、玻璃棒、量筒,还需要:______,若配制过程中定容时俯视刻度会使配制的浓度______(填偏大、偏小、不影响).
(2)步骤②脱色过程包括加入:______(填:脱有机色素的吸附剂名称)→搅拌煮沸→冷却→______(填操作).
(3)比色法确定待测液的浓度的原理是______
(4)已知有关离子的还原性顺序为I->Fe2+>SCN->Br->Cl-,则步骤②中Ⅲ可选择的氧化剂有______a.碘水 b.溴水 c.氯水 d.通入(SCN)2;写出加入上述某一氧化剂时涉及到的离子反应方程式:______
(5)若其补铁剂是由乳酸
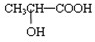
与铁粉作用生成的,请写出上述步骤②反应Ⅰ的化学方程式:______.
(1)反应操作步骤有量取、溶解、移液、洗涤、定容、摇匀等操作,首先用量筒量量取一定体积的溶液在烧杯中溶解,冷却后转移到25ml容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加;定容时,俯视容量瓶刻度线,使溶液的体积偏低,所以溶液浓度偏大,
故答案为:25mL容量瓶、胶头滴管;偏大;
(2)活性炭具有吸附性,可用来脱色,具有漂白性,脱色后,活性炭不溶于水,可用过滤的方法分离,故答案为:活性炭;过滤;
(3)溶液浓度越大,颜色越深,故答案为:溶液颜色与物质的量浓度成正比;
(4)由于离子的还原性顺序为I->Fe2+>SCN->Br->Cl-,所以溴水、氯水能将亚铁离子氧化为铁离子.加入氯水反应的离子方程式为Cl2+2Fe2+=2Fe3++2Cl-,
故答案为:bc;Cl2+2Fe2+=2Fe3++2Cl-;
(5)该补铁剂为乳酸亚铁[CH3CH(OH)COO]2Fe,乳酸具有弱酸性,利用强酸制弱酸.所以盐酸与乳酸亚铁[CH3CH(OH)COO]2Fe生成乳酸和氯化亚铁,反应方程式为[CH3CH(OH)COO]2Fe+2HCl→2CH3CH(OH)COOH+FeCl2,故答案为:[CH3CH(OH)COO]2Fe+2HCl→2CH3CH(OH)COOH+FeCl2.