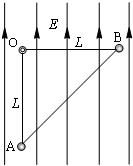
两个带电量均为+q的小球,质量均为m,固定在轻质绝缘等腰直角三角形框架OAB的两个端点A、B上,另一端点用光滑铰链固定在O点,整个装置可以绕垂直于纸面的水平轴在竖直平面内自由转动.直角三角形的直角边长为L.
(1)若施加竖直向上的匀强电场E1,恰能使框架OB边水平、OA边竖直并保持静止状态,则电场强度E1多大?在此电场中,框架能否停止在竖直平面内其它位置?
(2)若改变匀强电场的大小和方向(电场仍与框架平行),为使框架的OB边水平,A在O点的正下方,则所需施加匀强电场的场强E2至少多大?方向如何?
(3)若施加竖直向上的匀强电场E3=
,小球带电量分别变为qA=+2q,qB=+2mg q
q,其余条件不变.将框架从图示位置由静止释放,不计一切摩擦阻力,框架转动多少角度两个小球速度最大?并求出最大速度.5 2
(1)力矩平衡:qE1L=mgL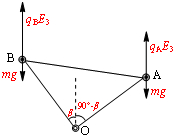
解出E1=mg q
电场力刚好抵消重力,故三角形框架能停止在竖直平面内任意位置.
(2)设E2与竖直方向成α角向右斜向上,
力矩平衡:qE2Lsinα+qE2Lcosα=mgL
解出E2=mg q(sinα+cosα)
因此,E2与竖直方向夹角为α=45°时,E2最小,
E2最小值E2min=
mg2 2q
(3)设OB边转到与竖直方向成β角时,合力矩为零:
qAE3Lcosβ-mgLcosβ+mgLsinβ-qBE3Lsinβ=0
解出tanβ=
,β=37°3 4
所以,框架转动90°+β=127°时,小球速度最大.
能量守恒定律:△E=△Ep+△Ek,
即:qAE3(L+Lsinβ)+qBE3Lcosβ=mg(L+Lsinβ)+mgLcosβ+2×
mvm21 2
解出vm=22gL
答:(1)若施加竖直向上的匀强电场E1,恰能使框架OB边水平、OA边竖直并保持静止状态,则电场强度E1为
.在此电场中,三角形框架能停止在竖直平面内任意位置.mg q
(2)若改变匀强电场的大小和方向(电场仍与框架平行),为使框架的OB边水平,A在O点的正下方,则所需施加匀强电场的场强E2至少为
,此时方向与竖直方向夹角为α=45°.
mg2 2q
(3)若施加竖直向上的匀强电场E3=
,小球带电量分别变为qA=+2q,qB=+2mg q
q,其余条件不变.将框架从图示位置由静止释放,不计一切摩擦阻力,框架转动127°两个小球速度最大,最大速度为25 2
.2gL
