用18mol/L浓硫酸配制480ml 1.0mol/L稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积②量取一定体积的浓硫酸③稀释④转移、洗涤⑤定容、摇匀
回答下列问题:
(1)所需浓硫酸的体积是______,量取浓硫酸所用的量筒的规格是______.
A、10ml B、25ml C、50ml D、100ml
(2)实验需要的仪器除容量瓶、烧杯、量筒外,还需要______.
(3)第③步实验的操作是______.
(4)下列情况对所配制的稀硫酸浓度有何影响(用偏大、偏小、无影响填写)
A、所用的浓硫酸长时间放置在密封不好的容器中______.
B、容量瓶用蒸馏水洗涤后残留有少量的水______.
C、未冷却至室温立即转移并定容______.
D、定容时俯视溶液的凹液面______.
(1)浓配制480mL1.0mol/L的稀H2SO4,需选择500mL容量瓶,根据稀释定律,稀释前后溶质的物质的量不变,来计算浓硫酸的体积,设浓硫酸的体积为xmL,则xmL×18mol/L=500mL×1.0mol/L,解得:x≈27.8,所以应量取的浓硫酸体积是27.8mL.
量取浓硫酸所用的量筒的规格是50mL.
故答案为:18.4mol/L; C.
(2)操作步骤有计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,用50mL量筒量取(用到胶头滴管)浓硫酸,在烧杯中稀释,用玻璃棒搅拌,冷却至室温后转移到500mL容量瓶中,并用玻璃棒引流,洗涤2-3次,将洗涤液转移到容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加至溶液凹液面与刻度线水平相切,盖好瓶塞颠倒摇匀.
所以需要的仪器为:玻璃棒、烧杯、胶头滴管、50 mL量筒、500mL容量瓶.
故答案为:玻璃棒、胶头滴管.
(3)浓硫酸稀释操作:把浓硫酸沿烧杯壁缓慢倒入盛水的烧杯中,不断用玻璃棒搅拌散热,防止溶液飞溅而烫伤操作者.
故答案为:用量筒量取27.8ml浓H2SO4,把浓硫酸沿烧杯壁缓慢倒入盛水的烧杯中,不断用玻璃棒搅拌散热,防止溶液飞溅而烫伤操作者.
(4)A、浓硫酸具有吸水性,浓硫酸长时间放置在密封不好的容器中,浓度会减小,量取的浓硫酸含有的溶质硫酸的物质的量减小,所配溶液浓度偏小;
B、最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响;
C、浓硫酸溶解后未冷至室温即进行转移、定容,一旦冷却下来会导致体积偏小,所配溶液浓度偏大;
D、定容时俯视刻度线,溶液体积偏小,所配溶液浓度偏大.
故答案为:偏小;无影响;偏大;偏大.

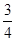 T时刻的波形曲线为( )
T时刻的波形曲线为( )