【物质结构与性质】(15分)
(1)已知X、Y、Z为同一短周期的三种元素,其原子的部分电离能(kJ/mol)如下表所示:
| X | Y | Z | |
| I1 | 496 | 738 | 577 |
| I2 | 4562 | 1451 | 1817 |
| I3 | 6912 | 7733 | 2754 |
| 9540 | 10540 | 11578 |
②写出Y原子的电子排布式_____________ Y的第一电离能大于Z的第一电离能的原因_______________________
③X晶体采用下列_________(填字母)堆积方式。
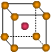
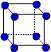
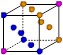
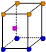
A B C D
(2)N2O的等电子体为:①分子______________,②阴离子______________;由此可知N2O的中心原子的杂化类型为_____________。根据价层电子对互斥模型确定NO2的分子构型为:_____________________________________。
(3)已知铜能形成多种化合物,如硫酸铜的结构如下图所示,
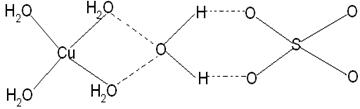
请在图中标出水合铜离子中的配位键.
(1)①Z>Y>X ②1s22s22p63s2 ;Y元素原子最外层s轨道上的电子为全满③A
(2)①CO2 ②SCN-或N3- ;SP 。V型
(3)
(1)①根据元素的电离能可知X是第IA,Y是第ⅡA,Z是第ⅢA。所以金属性是X>Y>Z。金属性越强,电负性越小,所以三种元素电负性大小关系为Z>Y>X。
②Y是镁,电子排布式为1s22s22p63s2。镁元素中3s轨道是全充满状态,稳定性强。
③X是钠,采用体心立方堆积,A正确,B是简单立方堆积,C是面心立方堆积,D是六方最密堆积,答案选A。
(2)电子数和原子数分别都相等的是等电子体,所以和N2O互为等电子体的是CO2、SCN-或N3-。N2O中心氧原子含有的孤对电子是(6-3×2)÷2=0,所以氧原子是sp杂化。NO2分子中的N以两个sp2杂化轨道与氧原子成键,形成V字型的空间构型,此外分子中还形成一个三中心三电子大∏键.
(3)水合铜离子中的配位键是由水分子提供孤对电子,铜离子提供空轨道,所以结构如图所示

