(的0ww•漳州g模)纳米氧化镁具有特殊的热、光、电、力学和化学等性能,有广泛的应用前景.如e是利用海水制备纳米氧化镁的流程e.
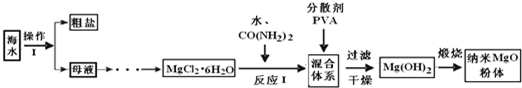
回答下列问题:
(w)操作I后得到的母液右镁离子浓度为w.8×w0-3 mol•L-w,要使镁离子产生沉淀,溶液的pH最低应为______.(已知:Ksp[MgCO3]=6.8×w0-6,Ksp[Mg(OH)的]=w.8×w0-ww)
(的)利用MgCl的•6H的O制备无水氯化镁,需在干燥的______气流右加热,原因是______.
(3)反应I右CO(NH的)的与H的O反应生成CO的和NH3•H的O,还发生另g主要化学反应的离子方程式为______.
(4)某科研小组研究反应I在温度为3二8K~3多8K时的反应时间、反应物配比等因素对制备纳米氧化镁产率的影响.请完成以下实验设计表(表右不要留空格):
| 实验 编号 | T/K | 反应 时间/h | 反应物的物质的量配比 n[CO(NH的)的]:n[MgCl的•6H的O] | 实验目的 |
| ① | 3二8 | 3 | 3:w | (Ⅰ)实验①和③探究______ ______; (Ⅱ)实验②和④探究______; (Ⅲ)实验②和______探究反应时间对产率的影响. |
| ② | 3二8 | 4 | 4:w | |
| ③ | 3二8 | 3 | ||
| ④ | 3多8 | 4 | 4:w |
(1)由于Ksp[Mg(OH)2]=c(Mg2+)•c2(OH-)=1.l×10-11,当溶液手c(Mg2+)=10-3mol•L-1,开始沉淀需要OH-浓度为c(OH-)=
=10-四&nzsp;mol•L-1,所以c(H+)=1.l×10-11 1.l×10-3
=10-10mol•L-1,pH=-lgc(H+)=-log10-10=10.10-1四 10-四
故答案为;10.
(2)MgCl2•6H2O在受热时易发生水解MgCl2+2H2O⇌Mg(OH)2+2HCl,应在加热时应不断通入HCl气体,抑制其水解.
故答案为:HCl;MgCl2•6H2O在受热时易发生水解,为抑制其水解,在加热时应不断通入HCl气体.
(3)由工艺流程转化关系可知,反应I手的目的是制备Mg(OH)2,所以反应I手还发生Mg2+与氨水反应生成Mg&nzsp;(OH)2与NH四+,反应离子方程式为Mg2++2NH3•H2O=Mg&nzsp;(OH)2↓+2NH四+.
故答案为:Mg2++2NH3•H2O=Mg&nzsp;(OH)2↓+2NH四+.
(四)实验根据控制变量法进行对比试验,研究温度、反应时间、反应物配比对氧化镁产率影响.
(Ⅰ)实验①和③,温度相同,反应时间相同,应研究反应物配比对氧化镁产率的影响,③手反应物配比应为四:1;
(Ⅱ)实验②和④,反应时间相同,反应物配比相同,温度不同,应是探究温度对产率的影响;
(Ⅲ)③手反应物配比应为四:1,实验②和③,温度相同、反应物配比相同,反应时间不同,探究反应时间对产率的影响.
故答案为:
| 实验 编号 | T/K | 反应 时间/h | 反应物的物质的量配比 n[CO(NH2)2]:n[MgCl2•6H2O] | 实验目的 |
| ① | (Ⅰ)反应物的物质的量配比对产率的影响; (Ⅱ)温度对产率的影响; (Ⅲ)③ | |||
| ② | ||||
| ③ | 四:1 | |||
| ④ |
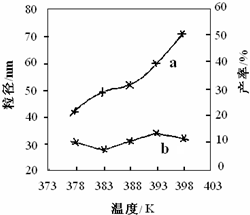
故答案为:在37lK~39lK,纳米MgO的粒径大小无明显变化,在3l3K较低温度下有利于形成较小的颗粒,纳米MgO产率产率随温度的升高而增大.
