实验室需用98ml1.0mol/L硫酸,现用浓硫酸(标签如下图)配制.实验仪器有:A.25ml量筒B.托盘天平C.玻璃棒D.50ml容量瓶E.10ml量筒F.胶头滴管G.50ml烧杯H.100ml容量瓶I.200ml容量瓶
(1)实验时应选用的仪器是(填入编号)______.
(2)所需浓硫酸的体积是______ml.
(3)下列错误操作可使所配制溶液浓度偏高的是______
A.容量瓶洗涤后未干燥
B.溶解搅拌时有液体飞溅
C.定容时俯视容量瓶瓶颈刻度线
D.摇匀后见液面下降,再加水至刻度线.

(1)配制步骤有量取、稀释、移液、洗涤、定容、摇匀等操作,一般用量筒量取浓硫酸在烧杯中稀释,冷却后转移到100mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器有玻璃棒、10ml量筒、胶头滴管、50ml烧杯、100ml容量瓶.
故选CEFGH.
(2)浓硫酸的物质的量浓度为:c=
=103ρw M
mol/L=18.4mol/L;设需要浓硫酸的体积为V,103×1.84×98% 98
1.0mol/L×0.1L=18.4mol/L×V,V=0.0054L=5.4mL,故答案为:5.4;
(3)A.所用容量瓶经蒸馏水洗涤后没有干燥,溶质的物质的量和溶液的体积都未改变,所以无影响;
B.溶解搅拌时有液体飞溅,导致溶质的物质的量偏小,所以配制溶液的浓度偏低;
C.定容时俯视容量瓶瓶颈刻度线,导致溶液的体积偏小,配制溶液的浓度偏高;
D.摇匀后发现液面低于刻度线,加入少量水至刻度线,溶液的体积偏大,导致配制溶液的浓度偏低;
故选C.

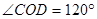 ,玻璃球对该激光的折射率为
,玻璃球对该激光的折射率为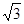 ,则下列说法中正确的是( )
,则下列说法中正确的是( )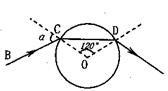
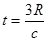 (c为真空中的光速)
(c为真空中的光速)