问题
实验题
为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)
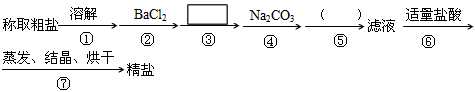
(1)判断BaCl2已过量的方法是_____________________。
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2) ;
___________________________________.
(3)在 中填写所使用除杂试剂的化学式__________,在( )中的操作名称是_______。
中填写所使用除杂试剂的化学式__________,在( )中的操作名称是_______。
(4)从实验设计方案优化的角度分析步骤②和④可否颠倒____________(填“是”或“否”,如果“否”,请说明理由。)原因是:_____________________;步骤③和④可否颠倒____________。
(5)若先用盐酸再进行操作⑤,将对实验结果产生影响,其原因是:____________________________
答案
(1)取第②步后的上层清液1~2滴于点滴板上(或取少量上层清液于试管中),再滴入1~2滴BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量(合理答案皆可)
(2)CaCl2+Na2CO3==CaCO3↓+2NaCl,BaCl2+Na2CO3==BaCO3↓+2NaCl
(3)NaOH;过滤
(4)否;过量的BaCl2必须要用Na2CO3除去; 是;
(5)会有部分沉淀溶解,从而影响制得精盐的纯度
