碳的化合物在工农业生产和生活中有广泛的应用。
已知CaC2与水反应生成乙炔。请回答下列问题:
①实验室制乙炔的反应方程式为 ;
②CaC2中C22—与O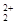 与互为等电子体,O22+的电子式可表示为 ;
与互为等电子体,O22+的电子式可表示为 ;
1 mol O22+中含有的π键数目为 (阿伏加德罗常数的值用NA表示);
③乙炔与氢氰酸反应可得丙烯腈(H2C=CH—C≡N)。丙烯腈分子中碳原子杂化轨道类型是 ,构成丙烯腈的元素中电负性最小的是 (填元素符号,下同),第一电离能最大的是 。丙烯腈分子中处于同一直线上的原子最多为 个,处于同一平面的原子为 个。
(8分)(1)①CaC2+2H2O→Ca(OH)2+C2H2↑
②[ ]2+ 2NA
]2+ 2NA
③sp、sp2杂化 H N 3 6
题目分析:①依据教材知识书写,方程式为CaC2+2H2O→Ca(OH)2+C2H2↑。
②带2个正电荷,失去2个电子,O22+的电子式可表示为[ ]2+。O22+中O和O原子含有3对共用电子,故1 mol O22+中含有的π键数目为2NA。
]2+。O22+中O和O原子含有3对共用电子,故1 mol O22+中含有的π键数目为2NA。
③第一个C原子和第二个碳原子是SP2杂化,第二个碳原子好第三个C原子是SP杂化。
点评:本题考查的是化学方程式的书写、电子式的书写和杂化轨道等综合知识,题目难度中,注意基础知识的学习、掌握及应用。

