碳是形成化合物最多的元素。
(1)由碳元素参与形成的物质多为分子晶体,也有少数原子晶体。下列关于分子晶体和原子晶体的说法正确的是 (填字母序号)。
A、完全由非金属元素形成的物质一定是分子晶体或原子晶体
B、分子晶体中分子之间一定存在范德华力
C、SiC具有极高的熔点和较大的硬度,SiC分子中除存在共价键外,还存在分子间作用力
D、金刚石是由碳元素形成的原子晶体,性质稳定,不与任何物质反应
(2)意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的C4分子。C4分子结构如图所示。下列说法正确的是 。
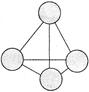
A、C4属于一种新型的化合物 B、C4与P4(白磷)的晶体都属于分子晶体
C、C4气体分子内含有极性共价键 D、C4与C60互为同素异形
(3)与碳同主族元素锗为32号元素,与锗同周期,且未成对电子数与锗相同,电负性最大的元素的价电子排布式为 。
(4)邻硝基苯酚的熔点 对硝基苯酚(填“>”、“=”或“<”=)。
(5)硼、碳、氮、氧是元素周期表第二周期相邻的四种元素。下列有关的四种化合物中,键角最小的是 。
A、CO2 B、CF4 C、NF3 D、OF2
已知硼酸H3BO3为白色固体,溶于水显弱酸性,但它却是一元酸,可以用硼酸在水溶液中的电离平衡解释它是一元弱酸的原因。
请写出下面这个方程式右端的两种离子的表达式:
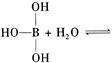 。
。
(6分)(1)B
(2)BD
(3)4s24p4
(4)<
(5)D 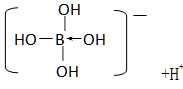
题目分析:(1)A项:NH4Cl是离子晶体,故错;C项:SiC是原子晶体,不存在分子间作用力,故错;D项:金刚石可以燃烧,故错。故选B。
(2)A项:C4是一种只由N元素组成的纯净物,为单质,故错;C项:C和C之间是非极性共价键,故错。故选BD。
(3)是硒元素,其价电子排布式为4s24p4。
(4)对-硝基苯酚分子间形成氢键,故邻硝基苯酚的熔点小于对硝基苯酚的熔点。
(5)A是180°,B是109°28′,C是120°,D是103.2°。故选D。
呈弱酸性,说明电离出了H+,故离子的表达式为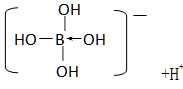 。
。
点评:本题考查的是晶体、化学键、子的核外电子排布、氢键、键角和电离平衡等综合知识,题目难度中,注意基础知识的学习、掌握和应用。
