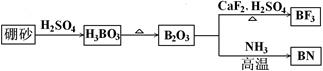
氮化硼(BN)是一种重要的功能陶瓷材料以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示:
请回答下列问题:
(1)由B2O3制备BF3、BN的化学方程式依次是
(2)在BF3分子中,F-B-F的键角是_______,B原子的杂化轨道类型为_______,BF3和过量NaF作用可生成NaBF4,BF4—的立体结构为_______;
(3)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为________,层间作用力为________;
(4)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm,立方氮化硼晶胞中含有______个氮原子、________个硼原子,立方氮化硼的密度是___________g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
(1)B2O3+3CaF2+3H2SO4D 2BF3+3CaSO4+3H2O B2O3+2NH3高温2BN+3H2O
(2) 120° sp2 正四面体 (3)共价键(极性共价键) 分子间力
(4)4 4 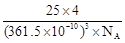
题目分析:(1)由B2O3制备BF3、BN的化学方程式依次是B2O3+3CaF2+3H2SO4D 2BF3+3CaSO4+3H2O 、 B2O3+2NH3高温2BN+3H2O;(2)在BF3分子中,中B原子为sp2杂化,其空间构型为平面三角形,B位于三角形的中央,故其键角为120°;BF3和过量NaF作用可生成NaBF4,此时B为sp3杂化,故BF4—的立体结构为正四面体;(4)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,金刚石为正四面体,硬度与金刚石相当,则该晶体为原子晶体,晶胞边长为361.5pm,所以立方氮化硼晶胞中含有4个氮原子,含有4个硼原子,立方氮化硼晶胞中含有4BN,B的相对原子质量为11,而N的相对原子质量为14,所以立方氮化硼的密度是: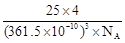 .
.
点评:本题考查了化学反应方程式的书写、杂化理论、化学键、晶胞的计算,该题的综合性好,本题难度中等。
