问题
选择题
a mol FeS与b mol FeO投入到VL、c mol/L的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为①(a+b)×189g ②Vc-(9a+b) mol ③(a+b)mol ④Vc-(9a+b)/3mol
A.①④
B.②③
C.①③
D.②④
答案
答案:A
由元素守恒知:未被还原的硝酸将转化为Fe(NO3)3中的NO3—,所以显酸性的硝酸的物质的量等于Fe(NO3)3的物质的量的3倍,由元素守恒知,n〔Fe(NO3)3〕=n(Fe)=(a+b)mol,所以未被还原的硝酸的质量="3(a+b)" mol×63 g·mol-1="(a+b)×189" g,①正确;
又根据化合价升降守恒知
a mol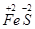 →a mol
→a mol 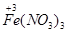 +a mol
+a mol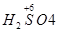 升高(3-2)a+(6+2)a="9a" mol
升高(3-2)a+(6+2)a="9a" mol
b mol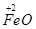 →b mol
→b mol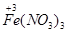 升高(3-2)b="b" mol
升高(3-2)b="b" mol
x mol  →x
→x 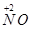 mol降低(5-2)x mol="3x" mol
mol降低(5-2)x mol="3x" mol
得9a mol+b mol=3xmol,即显氧化性的硝酸的物质的量x=(9a+b)/3mol,所以未被还原的硝酸为(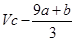 )mol,④正确
)mol,④正确
