问题
实验题
NaClO2用于棉、麻、粘胶纤维及织物的漂白。实验室制备NaClO2的装置如下图所示:
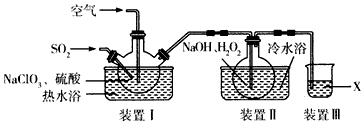
(1)装置I控制温度在35~55℃,通入SO2将NaClO3还原为ClO2(沸点:11℃),反应结束后通入适量的空气,其目的是____________________。
(2)装置Ⅱ中反应生成NaClO2的化学方程式为_______________。反应后的溶液中阴离子除了OH-外还可能含有的一种不含氯元素的阴离子是_______,检验该离子的方法是_______。
(3)已知在NaClO2饱和溶液中,温度低于38℃时析出的晶体是NaClO2·3H2O,温度高于38℃时析出的晶体是NaClO2,温度高于60℃时NaClO2分解生成NaClO3和NaCl。请补充从装置Ⅱ反应后的溶液中获得NaClO2晶体的操作步骤:
①减压,55℃蒸发结晶;②___________;③__________;④__________;⑤得到成品。
(4)装置Ⅲ中试剂X为______________。
答案
(1)将ClO2吹入到装置Ⅱ中进行反应
(2)2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2;SO42-;取少量反应后的溶液,先加足量的盐酸,无明显现象,再加BaCl2溶液,若产生白色沉淀,则说明含有SO42-
(3)②趁热过滤;③用38~60℃热水洗涤;④低于60℃干燥
(4)NaOH溶液
