实验室在蒸馏烧瓶中加NaBr、适量水、95%的乙醇和浓H2SO4,边反应边蒸馏,蒸出的溴乙烷用水下收集法获得。化学反应方程式为 NaBr+H2SO4=NaHSO4+HBr; C2H5OH+HBr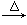 C2H5Br+H2O
C2H5Br+H2O
其中可能发生的副反应有 2HBr+H2SO4(浓)=Br2 +SO2↑+2H2O 已知CH3CH2Br的沸点为38.4℃,密度比水大,常温 下为不溶于水的油状液体。 请回答下列问题:
(1)反应中加入适量的水,除溶解NaBr外,作用还 有①_________;②____________。
(2)为了保证容器均匀受热和控制恒温,加热方法 最好采用___________。
(3)烧瓶中的导气管在瓶塞上的垂直部分比其他同 种装置中的导管要长些的原因是___________。
(4)本实验是否需要采用边反应边蒸馏的操作?_____________。
(5)溴乙烷可用水下收集法获得的依据和从水中分 离的方法是________。
(1)①吸收HBr ;②稀释浓硫酸,降低其氧化性,减少副产物
(2)水浴加热
(3)冷凝回流,减少反应物的损失,增大溴乙烷的浓度
(4)需要
(5)溴乙烷不溶于水且比水密度大,采用分液漏斗分液
