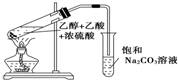
实验室用如图所示的装置制取乙酸乙酯
(1)在大试管中配制一定比例的乙醇.乙酸和侬硫酸的混合液的方法是______
(2)浓硫酸的作用是______.
(3)根据试管②中观察到的现象,可知乙酸乙酯的物理性质有______.
(4)试管②中饱和Na2CO3溶液的作用是______、______、______
(5)饱和Na2CO3溶液能否换成NaOH溶液______.为什么?______.(用化学方程式表示)
(6)试管②中的导气管不能插入溶液中,目的是防止 Na2CO3溶液倒吸.造成倒吸操作的原因是______.
(7)从试管②中分离出乙酸乙酯的实验操作是______.
(1)为防止酸液飞溅,应将密度大的液体加入到密度小的液体中.
故答案为:先加入一定量的乙醇,然后边振荡边加入浓硫酸.
(2)乙酸与乙醇在浓硫酸作催化剂加热条件下生成乙酸乙酯,由于反应为可逆反应,同时浓硫酸吸水有利于平衡向生成乙酸乙酯的方向移动.
故答案为:催化剂,吸水剂.
(3)实验观察到盛放饱和碳酸钠溶液试管中溶液分层,无色油状液体在上等现象.说明乙酸乙酯无色、不溶于水、密度比水小等.
故答案为:无色、不溶于水、密度比水小等.
(4)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,主要是利用了乙酸乙酯难溶于饱和碳酸钠,乙醇与水混溶,乙酸能被碳酸钠吸收,易于除去杂质.
故答案为:溶解乙醇;中和乙酸;降低乙酸乙酯的溶解度.
(5)乙酸乙酯在氢氧化钠溶液中完全水解,反应方程式为CH3COOCH2CH3+NaOH→CH3COONa+CH3CH2OH.
故答案为:不能;CH3COOCH2CH3+NaOH→CH3COONa+CH3CH2OH.
(6)加热不均匀易造成Na2CO3溶液倒流进加热反应物的试管中,导致试管破裂.
故答案为:加热不均匀.
(7)试管中液体不互溶,分层,所以用分液方法分离.
故答案为:分液.
