问题
实验题
某化学兴趣小组用如下装置模拟工业制备造纸原料BaSO3,并测定产品纯度。
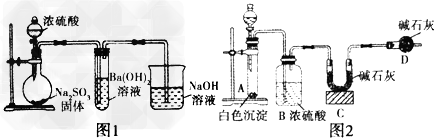
(1)图1烧瓶中发生反应的化学方程式为______________________________
(2)甲同学观察到图1试管中出现白色沉淀,该白色沉淀可能含有①BaSO3;②_________________________
(3)为探究白色沉淀的成分设计如下实验方案:

(4)为测定产品纯度取白色沉淀wg于图2装置的试管,在分液漏斗中加入____________(可从稀盐酸、稀硝酸、稀NaOH溶液中选择一种)。实验后,测得C装置增重mg,根据此实验数据可计算出白色沉淀中BaSO3的质量分数为__________(用含m、w的式子表示)。本测定方案有缺陷,请指出本方案的缺点及其对实验结果的可能影响 ________________________________________________
(5)为制备纯净的BaSO3,请设计改进图1装置的实验方案____________________。
答案
(1)Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+ H2O
(2)BaSO4
(3)稀盐酸;沉淀不完全溶解
(4)稀盐酸;因为盐酸挥发出来的HCl被C装置中碱石灰吸收,可能导致结果偏大;因为SO2 气体没有被完全吸收(部分SO2残留在装置中或SO2流速过快没有和C装置中的碱石灰完全反应等),可能导致结果偏小
(5)先从烧瓶的左边通入N2(CO2或稀有气体),排出装置中的空气
