四氯化钛是无色液体,沸点为136℃。它极易水解,遇空气中水蒸气即产生“白烟”(TiCl4+H2O=TiOCl2+2HCl↑)。在650℃~850℃下,将氯气通过二氧化钛和炭粉的混合物可得到四氯化钛和一种有毒气体。下图是某科研小组制备TiCl4的反应装置:其主要操作步骤如下:
①连接好整套装置,在通Cl2前先通入CO2气体并持续一段时间;
②当锥形瓶中TiCl4的量不再增加时,停止加热,从侧管中改通CO2气体直到电炉中的瓷管冷却为止;
③将TiO2、炭粉混合均匀后,装入管式电炉中;
④将电炉升温到800℃,一段时间后改通Cl2,同时在冷凝管中通冷凝水
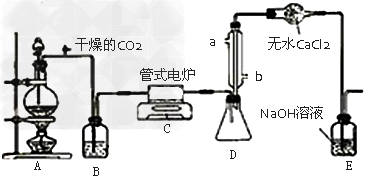
试回答下列问题:
(1)正确的操作顺序为________________(填序号)。
(2)C装置中的反应的化学方程式为________________。
(3)B中的试剂为_____________; 其作用是______________________。
(4)D装置的作用是_________________。
(5)干燥管中无水CaCl2的作用是__________________。
(6)从环境保护的角度,提出一个优化方案________________ 。
(1)③①④②
(2)TiO2 + 2Cl2 + 2C == TiCl4+ 2CO
(3)浓硫酸;干燥氯气
(4)冷凝四氯化钛
(5)防止E中的水蒸气进入D中 ,使TiCl4水解
(6)在尾气出口处加一点燃的酒精灯或增加一尾气处理装置
