实验室制乙酸乙酯得主要装置如图中A所示,主要步骤
①在a试管中按2∶3∶2的体积比配制浓硫酸、乙醇、乙酸的混合物;
②按A图连接装置,使产生的蒸气经导管通到b试管所盛的饱和碳酸钠溶液(加入几滴酚酞试液)中;
③小火加热a试管中的混合液;
④等b试管中收集到约2 mL产物时停止加热。撤下b试管并用力振荡,然后静置待其中液体分层;
⑤分离出纯净的乙酸乙酯。
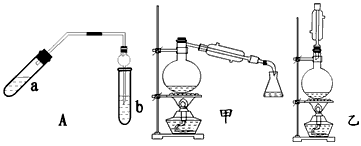
请回答下列问题:
(1)步骤①中,配制这一比例的混合液的正确操作是______________________。
(2)若实验中用含18O的乙醇与乙酸作用,该反应得化学方程式是:______________________。
(3)步骤③中,要用小火加热,其原因是______________________。
(4)步骤④中可观察到b试管中有细小的气泡冒出,写出该反应的离子方程式:__________________。
(5)A装置中使用球形管除起到冷凝作用外,另一重要作用是______________________,步骤⑤中分离乙酸乙酯必须使用的一种仪器是______________________。
(6)为充分利用反应物,甲、乙两位同学分别设计了图中甲、乙两个装置(乙同学待反应完毕冷却后,再用饱和碳酸钠溶液提取烧瓶中的产物)。你认为合理的是______________。
(1)在试管中加入3mL乙醇,然后边摇动边加入2mL浓硫酸和2 mL乙酸
(2)CH3CH218OH+CH3COOH
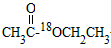 +H2O
+H2O
(3)防止温度过高,乙酸乙醇挥发溢出
(4)2CH3COOH+CO32-→2CH3COO-+H2O+CO2↑
(5)防止倒吸;分液漏斗
(6)乙
