学习化学知识后,要学会从化学视角观察物质世界.
(1)从组成角度看:世界上形形色色的物质都是由一百余种元素组合而成.水是由 组成的.
(2)从微粒角度看:构成物质的基本微粒有 .二氧化碳是由 构成的.
(3)从物质分类看:氢氧化镁可使酚酞溶液显红色,说明其具有 性.请写出其与盐酸反应的化学方程式 .
(4)从变化角度看:①化学变化中伴随着能量变化.甲烷燃烧的化学方程式是 ,反应同时伴随着将化学能转变为 能的过程.②在化学变化中,物质的转化遵循质量守恒定律.一定质量的某物质甲(相对分子质量是90)在氧气中完全燃烧,消耗6.4g氧气,同时生成5.6g一氧化碳、4.4g二氧化碳和5.4g水,则对甲的说法正确的是 (填字母序号).
A.只含有碳、氢两种元素
B.一定含有碳、氢元素,可能含有氧元素
C.碳元素质量分数为40%
D.若相同质量的甲在9.6g氧气中完全燃烧,则只生成二氧化碳和水.
(1)氢、氧(或H、O)
(2)分子、原子和离子 分子
(3)碱 Mg(OH)2+2HCl=MgCl2+2H2O
(4)①CH4+2O2 CO2+2H2O 热
CO2+2H2O 热
②CD
题目分析:(1)水是由氢氧元素组成,故答案:氢、氧(或H、O)
(2)分子、原子和离子是构成物质的三种微粒,多数物质由分子构成,金属单质、稀有气体、金刚石、石墨等由原子直接构成,酸碱盐由离子构成,故答案:分子、原子和离子 分子
(3)能使酚酞变红色的物质呈碱性,氢氧化镁和稀盐酸反应生成氯化镁和水,故答案:碱
Mg(OH)2+2HCl=MgCl2+2H2O
(4)①甲烷燃烧生成二氧化碳和水,释放热量,故答案:CH4+2O2 CO2+2H2O 热
CO2+2H2O 热
②A、从反应前后元素种类不变只能得出甲中一定含有碳、氢,可能含氧元素,A说法不正确.
B、5.6g一氧化碳中氧元素的质量为5.6g×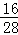 ×100%=3.2g,4.4g二氧化碳中氧元素的质量为4.4g×
×100%=3.2g,4.4g二氧化碳中氧元素的质量为4.4g×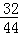 ×100%=3.2g,5.4g水中氧元素的质量为5.4g×
×100%=3.2g,5.4g水中氧元素的质量为5.4g×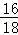 ×100%=4.8g,根据质量守恒定律反应前后氧元素的质量不变,反应后氧元素的总质量为3.2g+3.2g+4.8g=11.2g>6.4g,所以反应物甲中含有氧元素,氧元素的质量为11.2g﹣6.4g=4.8g.B说法不正确.
×100%=4.8g,根据质量守恒定律反应前后氧元素的质量不变,反应后氧元素的总质量为3.2g+3.2g+4.8g=11.2g>6.4g,所以反应物甲中含有氧元素,氧元素的质量为11.2g﹣6.4g=4.8g.B说法不正确.
C、5.6g一氧化碳中碳元素的质量为5.6g×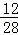 ×100%=2.4g,4.4g二氧化碳中碳元素的质量为1.2g,所以生成物中碳元素一共3.6g,根据质量守恒定律这与参加反应的甲中碳元素的质量相等,所以甲中碳元素的质量分数为
×100%=2.4g,4.4g二氧化碳中碳元素的质量为1.2g,所以生成物中碳元素一共3.6g,根据质量守恒定律这与参加反应的甲中碳元素的质量相等,所以甲中碳元素的质量分数为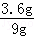 ×100%=40%,C正确.
×100%=40%,C正确.
D、设甲的化学式为CxHyOz,则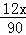 ×100%=40%,x=3;氧元素的质量分数为
×100%=40%,x=3;氧元素的质量分数为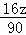 =
= ,z=3;根据甲的相对分子质量12×3+y+16×3=90,z=6;所以甲的化学式为C3H6O3,燃烧的化学方程式为C3H6O3+3O2
,z=3;根据甲的相对分子质量12×3+y+16×3=90,z=6;所以甲的化学式为C3H6O3,燃烧的化学方程式为C3H6O3+3O2 3CO2+3H2O,所以甲和氧气反应生成二氧化碳和水时甲和氧气的质量比为90:96,所以D说法正确.
3CO2+3H2O,所以甲和氧气反应生成二氧化碳和水时甲和氧气的质量比为90:96,所以D说法正确.
