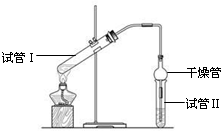
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室利用右图的装置制备乙酸乙酯.
(1)与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是:______.
(2)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用图所示装置进行了以下4个实验.实验开始先用酒精灯微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管II再测有机层的厚度,实验记录如下:
| 实验编号 | 试管Ⅰ中试剂 | 试管Ⅱ中试剂 | 测得有机层的厚度/cm |
| A | 3mL乙醇、2mL乙酸、1mL18mol•L-1 浓硫酸 | 饱和Na2CO3溶液 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 | |
| C | 3mL乙醇、2mL乙酸、6mL 3mol•L-1 H2SO4 | 1.2 | |
| D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
②分析实验______(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率.
③加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,可能的原因是______.
(1)球形干燥管容积较大,使乙酸乙酯充分与空气进行热交换,起到冷凝的作用,也可起到防止倒吸的作用,故答案为:冷凝,防倒吸;
(2)①本题是研究实验D与实验C相对照,证明H+对酯化反应具有催化作用的条件,题中采用了一个变量,实验C3mol•L-1 H2SO4,实验D盐酸,所以达到实验目的,实验D与实验C中H+的浓度一样,实验C3mL乙醇、2mL乙酸、3mol•L-1 H2SO4,实验D3mL乙醇、2mL乙酸、盐酸,要保证溶液体积一致,才能保证乙醇、乙酸的浓度不变,盐酸体积为6mL,实验D与实验C中H+的浓度一样,所以盐酸的浓度为6mol•L-1,故答案为:6,6;
②对照实验A和B可知:试管Ⅰ中试剂实验A比实验B多1mL18mol•L-1 浓硫酸,但是试管Ⅱ中试剂中测得有机层乙酸乙酯的厚度,实验A为5.0cm,而实验B只有0.1cm,故答案为:A;
③乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,CH3COOH+C2H5OH
CH3COOC2H5+H2O,该反应为可逆反应,实验发现温度过高,乙酸乙酯的产率反而降低,是由于乙酸、乙醇都易挥发,使产率降低,或因温度过高可能发生副反应使产率降低,如乙醇在140℃,在浓硫酸催化下脱水生成乙醚,浓硫酸 加热
故答案为:乙酸、乙醇都易挥发,温度过高可能使乙酸、乙醇大量挥发使产率降低,温度过高可能发生副反应使产率降低;
