水是生命之源,也是化学反应中的主角.请回答下列问题:
Ⅰ、氢气燃烧生成液态水热化学方程式是2H2(g)+O2(g)═2H2O(l)△H=-572kJ/mol,
(1)生成物能量总和______(填“大于”、“小于”或“等于”)反应物能量总和.
(2)若2mol氢气完全燃烧生成水蒸气,则放出的热量______572kJ(填“>”、“<”或“=”).
(3)氢气热值为______.
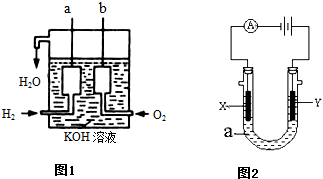
Ⅱ、氢气和氧气反应生成水,将化学能转化为电能,其构造如图1所示:a、b两个电极均由多孔的碳块组成,
(1)a电极反应式是______
(2)b电极反应式是______
Ⅲ、图2表示一个电解池.X、Y都是惰性电极,电解液a是饱和食盐水,同时在两边各滴入几滴酚酞试液.
(1)X极上的电极反应式为______,在X极附近观察到的现象是______.
(2)Y极上的电极反应式为______,检验该电极反应产物的方法是______.
Ⅰ(1)该反应正反应为放热反应,生成物的总能量小于反应物总能量,
故答案为:小于;
(2)气态水的能量高于液体水,故生成2mol气态水放出的热量小于572kJ,
故答案为:<;
(3)热值指1kg燃料完全燃烧放出的热量,由热化学方程式可知,1kg氢气燃烧放出的热量为
×572kJ=143000kJ,故氢气的热值为143000kJ/kg=143kJ/g,1000g 4g
故答案为:143kJ/g;
Ⅱ(1)a极通入氢气,发生氧化反应,在碱性条件下生成水,电极反应式为:H2+OH--2e-=2H2O,
故答案为:H2+OH--2e-=2H2O;
(2)b极通入氧气,发生还原反应,生成氢氧根,电极反应式为:O2+2H2O+4e-=4OH-,
故答案为:O2+2H2O+4e-=4OH-;
Ⅲ(1)X极连接电源的负极,为阴极,发生还原反应,氢离子在X极放电生成氢气,同时生成氢氧根,电极反应式为:2H2O+2e-=H2↑+2OH-,溶液呈碱性,故现象为:产生气泡,溶液变红色,
故答案为:2H2O+2e-=H2↑+2OH-;产生气泡,溶液变红色;
(2)Y极连接电源的正极,为阳极,发生氧化反应,氯离子在Y放电生成氯气,电极反应式为:2Cl--2e-=Cl2↑,用湿润的淀粉KI试纸检验,试纸变蓝,
故答案为:2Cl--2e-=Cl2↑;用湿润的淀粉KI试纸检验,试纸变蓝.
