问题
填空题
(1)一定温度下,在恒容密闭容器中NO2与O2反应如下:4NO2(g)+O2(g)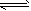 2N2O5(g)。若已知
2N2O5(g)。若已知
K350℃<K300℃,,则该反应是____(填“吸热”或“放热”)反应。反应达平衡后,若再通入一定量
NO2,则平衡常数K将____,NO2的转化率____。(均填“增大”“减小”或 “不变”)
(2)若初始时在恒容密闭容器中加入N2O5,下表为N2O5分解反应在一定温度下不同时间测得N2O5浓度的部分实验数据
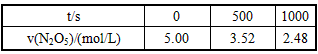
①写出该反应的平衡常数表达式:K=____。
②1000 s内N2O5的分解速率为____。
③若每有1 mol N2O5分解,放出或吸收Q kJ的热量,写出该分解反应的热化学方程式_______________。
答案
(1)放热;不变;变小
(2)①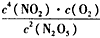 ;②0.00252 mol·L-1·s-1;③2N2O5(g)=4NO2(g) +O2(g) △H = +2Q kJ/mol
;②0.00252 mol·L-1·s-1;③2N2O5(g)=4NO2(g) +O2(g) △H = +2Q kJ/mol
