问题
计算题
晶须是一种发展中的高强度材料,它是一些非常细的,非常完整的丝状(横截面为圆形)晶体,现有一根铁晶,直径d="1.60" μm,用了F="0.0264" N的力将它拉断,试估算拉断过程
中最大的Fe原子力Ff.(Fe的密度ρ="7.92" g·cm-3).
答案
8.25×10-10 N
估算最大铁原子力,最关键之处就是要将已知的宏观量与待求的微观量如何相联系,这就要想到阿伏加德罗常数.
因原子力作用范围在10-10 m数量级,阻止拉断的原子力主要来自于断开面上的所有原子对.当Fe晶上的拉力分摊到一对Fe原子上的力超过拉伸中的最大原子力时,Fe晶就被拉断.又铁的摩尔质量
MA=55.85×10-3 kg/mol.
所以铁原子的体积:
V=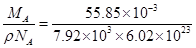 m3
m3
=1.171×10-29 m3
原子直径D=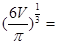 2.82×10-10 m
2.82×10-10 m
原子球的大圆面积S=πD2/4=6.25×10-20 m2
铁晶断面面积
S′=πd2/4=π×(1.60×10-6)2/4 m2=2.01×10-12 m2
断面上排列的铁原子数
N=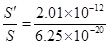 =3.2×107个
=3.2×107个
所以拉断过程中最大铁原子力
Ff=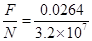 N=8.25×10-10 N.
N=8.25×10-10 N.
