(12分)某校化学小组学生利用“废铁屑与水反应”的产物还原氧化铜,并制取FeCl3·6H2O晶体。(图中夹持、加热及尾气处理装置均已略去)
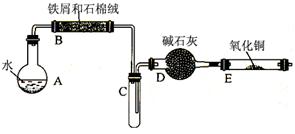
①将5%Na2CO3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去Na2CO3溶液,然后将废铁屑用蒸馏水洗涤2~3遍,用滤纸吸干水分。
②将洗涤干燥后的废铁屑和石棉绒混合置于气密性良好的上述装置B中。
③先点燃X处的酒精灯,待试管C中出现大量水雾时,点燃Y处的酒精喷灯。
④经过必要的实验操作后,点燃Z处的酒精灯。
⑤停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。
⑥利用上述滤液制取FeCl3·6H2O晶体,设计流程如下:
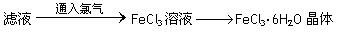
回答下列问题:
(1)实验步骤①的目的是 。
(2)步骤③X处是指 (用图中的A、B、C……表示),待试管C中出现大量水雾时,点燃Y处的酒精喷灯的目的是: 。
(3)步骤④必要的实验操作是指: 。
(4)步骤⑥从FeCl3溶液中得到FeCl3·6H2O晶体的主要操作包括:
。
(5)这个流程中需保持盐酸过量,主要原因是:
。
(每空2分,12分)
(1)除去废铁屑表面的油污(杂质)
(2)A 排除装置B中的氧气
(3)经验氢气的纯度
(4)加热浓缩,冷却结晶,过滤、洗涤
(5)过量盐酸能抑制FeCl3的水解
