回答下列问题
(1)画出磷原子的原子结构示意图:______.
(2)写出H2S分子的电子式:______.
(3)写出表示含有8个质子,10个中子的原子的化学符号:______.
(4)已知阴离子aXm-和阳离子bYn+具有相同的核外电子排布,则a、b、m、n之间的关系为a=______.
(5)用电子式表示氯化镁的形成过程:______.
(6)写出Na2O2中所含化学键的类型______.
(7)拆开1mol H-H键,1mol N-H键,1molN≡N键分别需要吸收的能量为436kJ,391kJ,946kJ:
则1mol N2完全转化成NH3______热量(填“吸收”或“放出”)______kJ;
(8)利用下列反应:Fe+Cu2+=Fe 2++Cu 制一个化学电池,写出电极反应式:
负极:______;正极______.
(1)根据核外电子层排布,磷原子的结构示意图为:
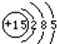
;故答案为
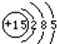
;
(2)H2S为共价化合物,电子式为
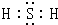
,故答案为:
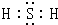
;
(3)因原子有8个质子,所以是氧元素,中子数为10,所以该原子表示为818O,故答案为:818O;
(4)因阳离子中:核电荷数=核外电子数+所带电荷数,阴离子中,核电荷数=核外电子数-所带电荷数.阳离子Xm-与阴离子Yn+的核外电子排布相同,即电子数相同,所以a+m=b-n,即a=b-n-m,故答案为:b-n-m;
(5)氯化镁是由1个镁原子和2个氯原子通过离子键形成的,形成过程为:

,
故答案为:

(6)因过氧化钠中既有钠离子和过氧根离子之间的离子键又有氧原子和氧原子之间的共价键,故答案为:离子键,非极性键;
(7)反应的方程式为:N2+3H2⇌2NH3,1molN2完全反应转化为NH3反应热为:946kJ+3×436kJ-6×391kJ=-92kJ,所以反应放出热量,故答案为:放出;92;
(8)工作时,正极反应式为Cu2++2e-=Cu,负极反应式为Zn-2e-=Zn2+,故答案为:Fe-2e-═Fe2+; Cu2++2e-═Cu
